
����Ŀ��A2+B2��2AB�ķ�Ӧ���̿��Կ������£���H��ʾ�ù��̵������仯����
��A2��A+A ��H1
��B2��B+B ��H2
��A+B��AB ��H3
������˵������ȷ����
A. ����H3+����H1+��H2����0ʱ���÷�Ӧ�����ȷ�Ӧ
B. ��2��H3+����H1+��H2����0ʱ���÷�Ӧ�Ƿ��ȷ�Ӧ
C. ��2��H3+����H1+��H2����0ʱ���÷�Ӧ�Ƿ��ȷ�Ӧ
D. ����H3+����H1+��H2����0ʱ���÷�Ӧ�����ȷ�Ӧ
 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������
��1�� ____��
____��
��2�� ____��
____��
��3��![]() ____��
____��
��4���л������� ������Ϊ____��____��
������Ϊ____��____��
��5��2��4����2��ϩд���ṹ��ʽ____________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���г�ҩ�������������ڶԿ� H1N1�����з����ش����ã�����Ч�ɷ���ԭ��Ľṹ��ʽ��ͼ�������й�˵���������
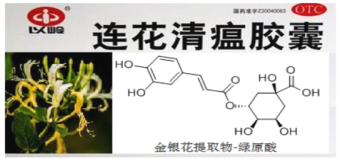
A. ��ԭ�����ڷ����廯����
B. ������������ 7 ��̼ԭ�ӹ���
C. 1mol ��ԭ���������� 5mol NaOH
D. ����ԭ�ᱽ����ȡ�������༰��������ͬ���л�����5 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A+3B=2C+2D��˵���������ֲ�ͬ����µķ�Ӧ����������
A. �ԣ�A��=0.25 mol/��L��min�� B. �ԣ�B��=0.6 mol/��L��min��
C. �ԣ�C��=0.5 mol/��L��min�� D. �ԣ�D��=0.6 mol/��L��min��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������֮������ϵ�������( )
A.12C��13C��Ϊͬλ��
B.(CH3)2CHCH2CH3��CH3CH2C(CH3)3��Ϊͬ���칹��
C.CH3CH3��CH3(CH2)3CH3��Ϊͬϵ��
D.O2��O3��Ϊͬ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ڹ���Ԫ���������̡�ͭ��п����̫���ܵ�ء����Բ��ϵȿƼ������й㷺��Ӧ�ã��ش��������⣺
��1�����ִ���ѧ�У�������______�ϵ���������������Ԫ�أ���Ϊ��������
��2��д�� Cu2+����Χ�����Ų�ʽ__________���Ƚ������̵ĵ���������(I3)����____��(���������� ��������������)��ԭ����________________��
��3����֪ [Zn(CN)4]2-���ȩ��ˮ��Һ�з�����Ӧ������һ�������� HOCH2CN�����ж���������̼ԭ�ӵ��ӻ���ʽ___________��1mol[Zn(CN)4]2-�е� �� ����Ϊ__________��
��4����ͼ�Ǿ��� Fe3O4 �ľ������þ�����һ�ִ��Բ��ϣ� �ܵ��硣
�������ж��������Ӵ���������Χ�ɵ�______(��ռ�ṹ)��϶��
�������������ӵĶѻ���ʽ��ij��������ԭ�Ӷѻ���ʽ��ͬ���öѻ���ʽ����Ϊ________��
������ Fe3O4 �����ܵ����ԭ��_________________������������Խ��߳�Ϊ a nm���� Fe3O4 ������ܶ�Ϊ________g��cm��3(�����ӵ������� NA ��ʾ)��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��º��ݵ��ܱ�������ͨ��lmolX��2molY���������з�Ӧ:X(g)+2Y(g)![]() M(g)+2N(g) ��H=akJ/mol(a>0)������˵������ȷ����
M(g)+2N(g) ��H=akJ/mol(a>0)������˵������ȷ����
A. ����ƽ��״̬ʱ�����������ƽ�ⲻ�ƶ�����Ӧ����Ҳ���ᷢ���ı�
B. ��Ӧ�ﵽƽ��ʱ��X��Y��ת�������
C. v��(X)=2v��(N)ʱ����Ӧ����ƽ��״̬
D. ����ƽ��״̬ʱ����Ӧ����akJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijԪ��B�ĺ˵����ΪZ����֪Bn-��Am+�ĺ��������ͬ�ĵ��Ӳ�ṹ����AԪ�ص�ԭ��������Z��n��m����ʾ��ӦΪ�� ��
A.Z+n��mB.Z��n+mC.Z��n��mD.Z+m+n
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ҳ��Ħ����������Ϊƽ��Ħ�����������ţ�![]() �������¹���
�������¹���![]() ���㷨�������
���㷨�������
A. ij��������ڱ�״�����ܶȦ�=1.429g/L����û�������![]() =32g/mol
=32g/mol
B. ��֪ijCO��CO2��ɵĻ�������![]() =30g/mol����CO��CO2�������Ϊ7:1
=30g/mol����CO��CO2�������Ϊ7:1
C. ��֪��Ӧ��(NH4)2CO3 ![]() 2NH3�� + H2O�� + CO2����һ������(NH4)2CO3������ȫ�ֽ�����û�����壨�¶�200��C�£���
2NH3�� + H2O�� + CO2����һ������(NH4)2CO3������ȫ�ֽ�����û�����壨�¶�200��C�£���![]() =26.3g/mol
=26.3g/mol
D. һ���¶Ⱥ�ѹǿ�£��������ܶ��������ܶȵ�14.3�������ʱ����![]() =28.6g/mol
=28.6g/mol
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com