
【题目】在FeCl3、CuCl2和HCl的混合溶液中加入铁粉,待反应结束后,将剩余的固体滤出,发现固体能被磁铁吸引,则反应后溶液中大量存在的阳离子是
A. Fe2+ B. H+ C. Cu2+和Fe2+ D. Fe3+和Cu2+
科目:高中化学 来源: 题型:
【题目】下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO43-+2I-+2H+![]() AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒.甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液.下列叙述中正确的是( )
AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒.甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40%NaOH溶液.下列叙述中正确的是( )
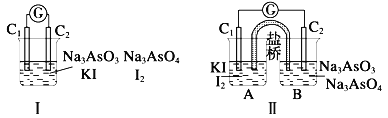
A.甲组操作时,微安表(G)指针发生偏转
B.甲组操作时,溶液颜色变深
C.乙组操作时,C1上发生的电极反应为I2+2e-═2I-
D.乙组操作时,C2做正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的离子,能在溶液中大量共存的是
A.NO3―、Ag+、H+、Cl― B.CO32―、Na+、Ca2+、NO3―
C.Mg2+、Cl―、OH―、CH3COO― D.Mg2+、SO42―、K+、Cl―
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中的杂质(括号内是杂质),能采用加入过量NaOH溶液充分反应再过滤的方法的是
A. Fe2O3(Al2O3) B. KCl(NaCl) C. SiO2(CaCO3) D. FeCl2溶液(FeCl3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)可逆反应:N2O4![]() 2NO2,在体积不变的密闭容器中反应,下列说法中可判断该反应达到平衡状态的是 (选填序号)
2NO2,在体积不变的密闭容器中反应,下列说法中可判断该反应达到平衡状态的是 (选填序号)
①单位时间内生成2nmolNO2的同时生成n mol N2O4
②单位时间内消耗n mol N2O4的同时生成2n mol NO2
③容器中的压强不再改变的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
(2)373k时把0.12 mol无色的N2O4气体通入体积500 ml的密闭容器中,发生反应:
N2O4![]() 2NO2,容器中立即出现红棕色。反应进行到2s时,测得生成NO2的物质的量为0.01 mol;反应进行到60 s时达到平衡,此时容器内N2O4与NO2的物质的量相等。请计算: (本小题要求写出解过程)
2NO2,容器中立即出现红棕色。反应进行到2s时,测得生成NO2的物质的量为0.01 mol;反应进行到60 s时达到平衡,此时容器内N2O4与NO2的物质的量相等。请计算: (本小题要求写出解过程)
①开始2 s内以N2O4表示的化学反应速率;
②达到平衡时体系的压强与开始时体系的压强之比;
③达到平衡时,体系中NO2的物质的量浓度;
④N2O4的平衡转化率。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
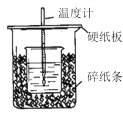
(1)从实验装置上看,图中尚缺少的一种玻璃用品是_____________________。
(2)烧杯间填满碎纸条的作用是_____________________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值__________(填“偏大、偏小、无影响”)
(4)该同学所用的装置,有一处明显不合理,请你说明不合理之处:____________________。
(5)在实验过程中,该同学没有找到缺少的那一件用品,就用铁丝自己做了一个,你认为______(填“是、否)可以,请说明原因_____________________。
(6)实验中改用60 mL 0.50 mol·L-1的盐酸跟50 mL 0.55 mol·L-1的NaOH溶液进行反应,与上述实验相比,所求中和热_________ (填“相等”或“不相等”),所放出的热量_________(填“相等”或“不相等”)。
(7)用相同浓度和体积的醋酸(CH3COOH)代替盐酸溶液进行上述实验,测得的中和热的数值会___________;(填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2(g)+1/2O2(g)![]() SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= -99kJ·mol-1.请回答下列问题:
SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= -99kJ·mol-1.请回答下列问题:
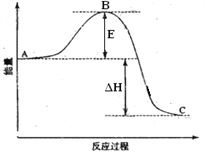
(1)图中可知A、C分别表示______________、_______________;E的大小对该反应的反应热有无影响?___________。
(2)图中△H=______________;
(3)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成5molSO3(g)的△H=______kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中一定能判断某化学平衡发生移动的是( )
A. 混合物中各组分的浓度改变 B. 正、逆反应速率改变
C. 混合物中各组分的含量改变 D. 反应物的转化率改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com