
| 酸 | 电离常数 |
| 碳酸 | K1=4×10-7 K2=5.6×10-11 |
| 亚硫酸 | K1=1.54×10-2 K2=1.02×10-7 |
 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源:不详 题型:单选题
| A.0.1 mol·L-1氨水,溶液的pH=13 |
| B.0.1 mol·L-1氨水加水稀释,溶液中c(H+)和c(OH-)都减小 |
| C.0.1 mol·L-1醋酸溶液中:c(H+)=c(CH3COO-) |
| D.0.1 mol·L-1醋酸与0.1 mol·L-1NaOH溶液等体积混合所得溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
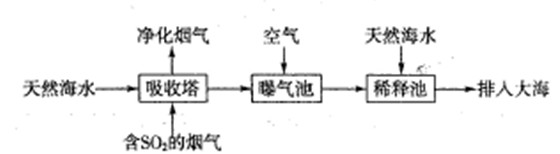
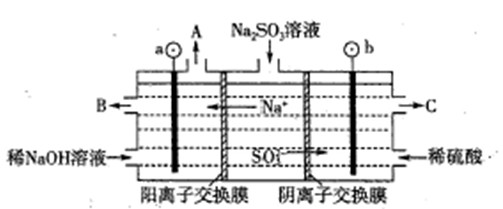
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
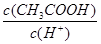 ④
④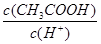 ⑤c(OH-) ⑥c(CH3COO-)
⑤c(OH-) ⑥c(CH3COO-)| A.①②③ | B.②③⑤ | C.④⑤ | D.④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
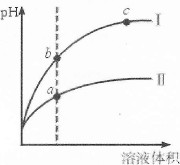
| A.Ⅱ为盐酸稀释时的pH变化曲线 |
| B.b点溶液的导电性比c点溶液的导电性强 |
| C.a点Kw的数值比c点Kw的数值大 |
| D.b点酸的总浓度大于a点酸的总浓度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| pH | c(CrO42—) | c(HCrO4—) | c(Cr2O72—) | c(H2CrO4) |
| 4 | 0.0003 | 0.1040 | 0.4480 | 0 |
| 6 | 0.0319 | 0.0999 | 0.4370 | 0 |
| 7 | 0.2745 | 0.0860 | 0.3195 | 0 |
| 9 | 0.9960 | 0.0031 | 0.0004 | 0 |
 H++HCrO4—
H++HCrO4—查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溶液中导电粒子的数目减少 |
B.溶液中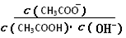 不变 不变 |
| C.醋酸的电离程度增大,c(H+)亦增大 |
| D.再加入10 mL pH=11的NaOH溶液,混合液pH <7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HX可能是强酸 |
| B.HX的酸性比HY的酸性弱 |
| C.两酸的浓度大小[HX]<[HY] |
| D.pH=1的两种一元酸均稀释100倍,稀释后两溶液的pH均为3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 醋酸浓度(mol/L) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com