

| ||
| ||
| ||
| ||
 ���Ȼ����ڷ�Ӧ�мȱ��������ֱ��ֻ�ԭ�ԣ�4mol�Ȼ���μӷ�Ӧ������Ϊ���Ե�ռ
���Ȼ����ڷ�Ӧ�мȱ��������ֱ��ֻ�ԭ�ԣ�4mol�Ȼ���μӷ�Ӧ������Ϊ���Ե�ռ| 1 |
| 2 |
| 22.4L |
| 22.4L/mol |
 ��2mol��
��2mol��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ʯ�͵��ѻ����ѽ���Եõ�ϩ�� |
| B��ʯ�͵Ĵ������ǻ�÷���������Ҫ;�� |
| C��ʯ�ͷ�����ĸ���־��Ǵ����� |
| D��ú���������ú���;�����ɵõ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� �� �� |
| B�������2��2-�������� |
| C���Ҷ����ͱ����� |
| D��1��1-���������1��2-�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | Na2CO3 | NaHCO3 | Na2SiO3 | Na2SO3 | NaHSO3 | NaClO |
| pH | 11.6 | 9.7 | 12.3 | 10.0 | 4.0 | 10.3 |
| A������������HCO3-��HSO3-��HClO |
| B�����H+��������SiO32-��CO32-��SO32- |
| C��6����Һ�У�Na2SiO3��Һ��ˮ�ĵ���̶���С |
| D����Ҫ�������Ʊ�����ˮ��HClO��Ũ�ȣ��������м���Na2SiO3��Na2SO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ5��6 |
| B��������ɫ������ԭ�������ɵ�P2O5��ɫ����С�������̣���ˮ�Ժ�ǿ�����տ����е�ˮ�֣���������СҺ�Σ����� |
| C��������Ӧ������3 mol Pʱ��ת�Ƶ��ӵ����ʵ���Ϊ10mol |
| D��������ҩ�еĺ������ð��״��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH3-CH2-CH2-OH |
| B��CH3-CH2-OH |
C��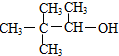 |
D��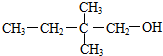 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� ��Ӧ������������ϵ������ͼ��ʾ |
| B����H��ֵ�뷴Ӧ����ʽ�ļ���ϵ���й� |
| C�������÷�Ӧ��Ƴ�ԭ���пΪ���� |
| D�����������Ϊԭ��ص���32.5gп�ܽ�ʱ�������ų�����һ��Ϊ11.2L |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com