
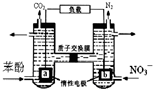
 我国科学家构建了一种双室微生物燃料电池,以苯酚(C6H6O)为燃料,同时消除酸性废水中的硝酸盐.下列说法正确的是:( )
我国科学家构建了一种双室微生物燃料电池,以苯酚(C6H6O)为燃料,同时消除酸性废水中的硝酸盐.下列说法正确的是:( )| A. | a为正极 | |
| B. | 若右池产生0.672L气体(标况下),则转移电子0.15mol | |
| C. | 左池电极反应式为C6H6O+11H2O-28e-═6CO2↑+28H+ | |
| D. | 左池消耗的苯酚与右池消耗的NO3-的物质的量之比为28:5 |
分析 该原电池中,硝酸根离子得电子发生还原反应,则右边装置中电极b是正极,电极反应式为2NO3-+10e-+12H+=N2↑+6H2O,左边装置电极a是负极,负极上C6H6O失电子发生氧化反应生成二氧化碳,电极反应式为C6H6O+11H2O-28e-=6CO2↑+28H+,据此分析解答.
解答 解:该原电池中,硝酸根离子得电子发生还原反应,则右边装置中电极b是正极,电极反应式为2NO3-+10e-+12H+=N2↑+6H2O,左边装置电极a是负极,负极上C6H6O失电子发生氧化反应生成二氧化碳,电极反应式为C6H6O+11H2O-28e-=6CO2↑+28H+,
A.该原电池中,左边装置电极a是负极,故A错误;
B.右边装置中电极b是正极,电极反应式为2NO3-+10e-+12H+=N2↑+6H2O,产生0.672L气体(标况下),则转移电子$\frac{0.672L}{22.4L/mol}$×10=0.3mol,故B错误;
C.左边装置电极a是负极,负极上C6H6O失电子发生氧化反应生成二氧化碳,电极反应式为C6H6O+11H2O-28e-=6CO2↑+28H+,故C正确;
D.放电时,右边装置中电极b是正极,电极反应式为2NO3-+10e-+12H+=N2↑+6H2O,左边装置电极a是负极,电极反应式为C6H6O+11H2O-28e-=6CO2↑+28H+,根据得失电子守恒,则消耗的苯酚与右池消耗的NO3-的物质的量之比为5:28,故D错误;
故选C.
点评 本题考查化学电源新型电池,侧重考查学生获取信息、分析推断能力,根据N元素化合价变化确定正负极,难点是电极反应式的书写,且原电池和电解池原理是高考高频点,要熟练掌握.


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:选择题
| A. | 煤炭经气化、液化和干馏等过程,可获得清洁能源和重要的化工原料 | |
| B. | 机动车实行限行措施是减少雾霾的途径之一 | |
| C. | 日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应 | |
| D. | 神舟10号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是单晶硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7个 | B. | 9个 | C. | 19个 | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X2+2Y2=2Z | B. | 2X2+2Y2=2Z | C. | 3X2+Y2=2Z | D. | X2+3Y2=2Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放热反应的反应速率一定大于吸热反应的反应速率 | |
| B. | 熔融状态下能导电的化合物一定含离子键 | |
| C. | 增大反应物浓度可加快反应速率,因此可用浓硫酸与锌反应增大生成氢气的速率 | |
| D. | 是否有丁达尔现象是胶体和溶液的本质区别 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 | |
| B. | 实验室常采用铁屑、溴水、苯混合制溴苯 | |
| C. | 苯中含有少量的苯酚可先加适量的浓溴水,使之生成三溴苯酚,再过滤除去 | |
| D. | 一定物质的量浓度溶液的配置必须要用干燥的容量瓶,否则有误差 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验目的 | |
| A | 将卤代烃加入到热NaOH溶液中一段时间后,取上层液体,加入AgNO3液产生沉淀 | 证明卤代烃中含有卤元素 |
| B | 电石与水反应制得的气体直接通往酸性KMnO4溶液 | 证明制得的气体是否为乙炔 |
| C | 淀粉在硫酸催化作用下水解,将新制氢氧化铜悬浊液加入到水解后的溶液中 | 检验淀粉水解的产物葡萄糖 |
| D | 向纯碱中滴加醋酸,将产生的气体先通入饱和碳酸氢钠溶液再通入苯酚钠浓溶液 | 证明酸性:醋酸>碳酸>苯酚 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com