
A、已知质量的铝镁合金,通过下面实验设计可以测定镁的质量分数:铝镁合金
| ||
| B、在配制一定物质的量浓度的溶液时,先称量或量取物质,再溶解或稀释,并将溶液转移至容量瓶,洗涤烧杯和玻璃棒并将洗涤液转移到容量瓶,继续往容量瓶中加水至溶液的凹液面正好与刻度线相切 | ||
| C、用裂化汽油萃取溴水中的溴之后进行分液时,水层从分液漏斗的下口放出 | ||
| D、欲检验SO2中是否混有CO2,可将该气体依次通过盛有饱和碳酸氢钠溶液、品红溶液、澄清石灰水的洗气瓶,若品红溶液不褪色且澄清石灰水变浑浊,则证明混有CO2 |


科目:高中化学 来源: 题型:
| A、常温下,0.1 mol碳酸钠晶体中含有CO32-的数目小于0.1 NA |
| B、36g CaO2中含有的离子数目为0.15 NA |
| C、100g 98%的浓硫酸中,氧原子总数为4NA |
| D、标准状况下,14.2g氯气与足量石灰乳充分反应转移电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHS在水中的电离方程式为:NaHS═Na++HS-和HS-═H++S2- |
| B、同物质的量浓度的氨水和盐酸反应至中性时所用体积:V(NH3?H2O)>V(HCl) |
| C、Na2SO3溶液中:c(H+)+c(HSO3-)+2c(H2SO3)=c(OH-) |
| D、同浓度的下列溶液中,c(CH3COO-)的大小:CH3COONa>CH3COONH4>CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜-锌-稀硫酸组成的原电池中,锌为正极 |
| B、铜-锌-稀硫酸组成的原电池中,电解质溶液的质量逐渐减轻 |
| C、用石墨电极电解CuCl2溶液时,阳极上Cu2+放电而析出金属铜 |
| D、用石墨电极电解CuCl2溶液时,电解质溶液的浓度逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(N2):v(H2):v(NH3)=1:3:2 |
| B、c(N2):c(H2):c(NH3)=1:3:2 |
| C、容器内混合气体的平均相对分子质量不变 |
| D、单位时间里每增加1molN2,同时增加3molH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡 常数(25℃) |
1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
| A、等物质的量浓度的各溶液pH关系为pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) |
| B、amol?L-1HCN溶液与amol?L-1NaOH溶液等体积混合后,所得溶液显碱性(pH>7),则c (OH-)>c(H+),c(Na+)>c(CN-) |
| C、冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小 |
| D、NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
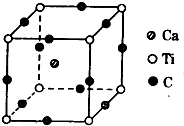 短周期元素A、B、C、D,A元素的原子最外层电子排布式为ms1,B元素的原子价电子排布式为ns2np2,C元素位于第二周期且原子中p亚层与所有s亚层电子总数相等,D元素原子的L层的p亚层中有3个未成对电子.
短周期元素A、B、C、D,A元素的原子最外层电子排布式为ms1,B元素的原子价电子排布式为ns2np2,C元素位于第二周期且原子中p亚层与所有s亚层电子总数相等,D元素原子的L层的p亚层中有3个未成对电子.查看答案和解析>>
科目:高中化学 来源: 题型:
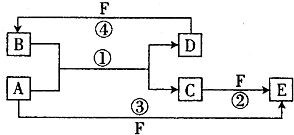
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com