
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 放热的反应在常温下一定很容易发生 | |
| C. | 吸热反应发生过程中要不断从外界获得能量,放热反应不需要吸收外界能量 | |
| D. | 是放热反应还是吸热反应主要由反应物、生成物所具有的总能量的相对大小决定 |
科目:高中化学 来源: 题型:解答题
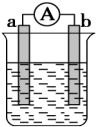 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:
如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
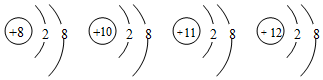
| A. | 它们属于不同种元素 | |
| B. | 它们的核外电子排布相同 | |
| C. | 它们都是离子 | |
| D. | 它们都具有稀有气体原子的稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和氧气 | B. | 锌和硫酸 | ||
| C. | 氢氧化钠和二氧化碳 | D. | 氢气和氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | ||
| V/mL | c/(mol•L-1) | V/mL | c/(mol•L-1) | ||
| A | 25 | 5 | 0.1 | 20 | 0.1 |
| B | 25 | 5 | 0.2 | 10 | 0.2 |
| C | 35 | 5 | 0.1 | 20 | 0.1 |
| D | 35 | 5 | 0.2 | 10 | 0.2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含lmolH2SO4的浓硫酸与足量铜在加热条件下反应,转移的电子总数为NA | |
| B. | 0.1 L0.5mol/LCH3COOH 溶液中含有的氢离子为0.05NA | |
| C. | 粗铜精炼时阳极质量减少6.4g,则外电路上通过0.2NA电子 | |
| D. | 1molCH3COONa和少量CH3COOH溶于水所得到的中性溶液中,CH3COO-的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14C与12C是两种不同的元素或核素 | |
| B. | 通过化学变化可以实现16O与18O之间的相互转化 | |
| C. | 35Cl2与37Cl2互为同素异形体 | |
| D. | 铯元素的两种同位素中137Cs比133Cs多4个中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②④⑤ | C. | ①④⑤ | D. | ①②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com