
有关晶体的下列说法中正确的是( )
A.晶体中分子间作用力越大,分子越稳定
B.原子晶体中共价键越强,熔点越高
C.冰熔化时水分子中共价键发生断裂
D.氯化钠熔化时离子键未被破坏
科目:高中化学 来源:2015-2016学年山东省高一6月月考化学试卷(解析版) 题型:选择题
下列属于吸热反应的是( )
①液态水汽化
②将胆矾加热变为白色粉末
③苛性钠溶于水
④氯酸钾分解制氧气
⑤生石灰跟水反应生成熟石灰
⑥干冰升华
A.①④ B.②④ C.③⑤ D.④⑥
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省成都市高一下4月月考化学试卷(解析版) 题型:选择题
运用元素周期律分析下面的推断,其中错误的是:①铍(Be)的氧化物的水化物可能具有两性,②铊(Tl)既能与盐酸作用产生氢气,又有跟NaOH溶液反应放出氢气,③砹(At)为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀硝酸,④锂(Li)在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱,⑤硫酸锶(SrSO4)是难溶于水的白色固体,⑥硒化氢(H2Se)是无色,有毒,比H2S稳定的气体( )
A. ①②③④ B. ②④⑥ C. ①③⑤ D. ②④⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省成都市高二下4月月考化学试卷(解析版) 题型:填空题
对金属制品进行抗腐蚀处理,可延长其使用寿命.
(1)以下为铝材表面处理的一种方法:
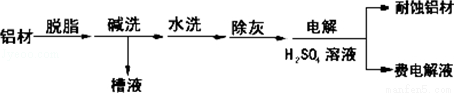
①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,用离子方程式表示其原因 .为将碱洗后槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的 (填字母序号).
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极的电极反应式为 .
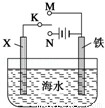
(2)利用图装置,可以模拟铁的电化学防护.若X为碳棒,为减缓铁的腐蚀,开关K应置于 处.
若X为锌,开关K置于M处,该电化学防护法称为 .
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省成都市高二下4月月考化学试卷(解析版) 题型:选择题
在通常条件下,下列各组物质的性质排列正确的是( )
A.熔点:CO2>KCl>SiO2
B.水溶性:HCl>H2S>SO2
C.沸点:CH3OCH3>CH3CH2OH
D.热稳定性:HF>H2O>NH3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省成都市高二下4月月考化学试卷(解析版) 题型:选择题
现有四种元素的基态原子的电子排布式如下:
①1s22s22p63s23p4②1s22s22p63s23p3③1s22s22p3④1s22s22p5
则下列有关比较中正确的是( )
A.第一电离能:④>③>②>①
B.原子半径:④>③>②>①
C.电负性:④>③>②>①
D.最高正化合价:④>③=②>①
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西大学附中高二下3月月考化学试卷(解析版) 题型:填空题
新材料的出现改变了人们的生活,对新材料的研究越来越重要.
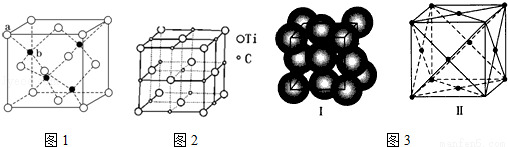
(1)硫化锌在荧光体、光导体材料、涂料、颜料等行业中应用广泛.其晶胞结构如图1所示,a位置是S2﹣、b位置Zn2+则此晶胞中含有 个S2﹣,Zn2+的配位数为 .
(2)最近发现一种钛原子和碳原子构成的气态团簇分子,如图2所示,项角和面心的原子是钛原子,棱的中心和体心的原子是碳原子,它的化学式为 .
(3)由甲烷分子,在一定条件下可以得到“碳正离子”CH3+,和“碳负离子”CH3﹣,CH3+中C﹣H键键角是 ;CH3﹣的空间构型是 .
(4)某金属材料的结构如图3﹣I所示,属于面心立方的结构,晶胞结构如图3﹣Ⅱ所示.
若晶胞的边长为a pm,金属的密度为ρ g/cm3,金属的摩尔质量为M g/mol,则阿伏加德罗常数NA= mol﹣1.
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西大学附中高二下3月月考化学试卷(解析版) 题型:选择题
下列物质中,难溶于CCl4的是( )
A.碘单质 B.氯化氢 C.苯 D.甲烷
查看答案和解析>>
科目:高中化学 来源:2016年全国普通高等学校招生统一考试化学(天津卷精编版) 题型:填空题
下表为元素周期表的一部分。
碳 | 氮 | Y |
|
X |
| 硫 | Z |
回答下列问题
(1)Z元素在周期表中的位置为__________。
(2)表中元素原子半径最大的是(写元素符号)__________。
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是__________。
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)X与Z两元素的单质反应生成1molX的最高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出该反应的热化学方程式:__________。
(5)碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9∶1,烃的电子式为__________。Q与水反应的化学方程式为__________。
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol/LNaOH溶液和1molO2,则两种气体的分子式及物质的量分别为__________,生成硫酸铜物质的量为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com