
·“Ó¦¢Ł”¢¢Ś·Ö±šŹĒ“Óŗ£Ōå»ŅŗĶijÖÖæóŹÆÖŠĢįČ”µāµÄÖ÷ŅŖ·“Ó¦£ŗ
¢Ł2NaI£«MnO2£«3H2SO4=2NaHSO4£«MnSO4£«2H2O£«I2
¢Ś2NaIO3£«5NaHSO3=2Na2SO4£«3NaHSO4£«H2O£«I2
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
| A£®Į½øö·“Ó¦ÖŠ¾łĪŖĮņŌŖĖŲ±»Ńõ»Æ |
| B£®µāŌŖĖŲŌŚ·“Ó¦¢ŁÖŠ±»»¹Ō£¬ŌŚ·“Ó¦¢ŚÖŠ±»Ńõ»Æ |
C£®Ńõ»ÆŠŌ£ŗMnO2£¾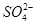 £¾ £¾ £¾I2 £¾I2 |
| D£®·“Ó¦¢Ł”¢¢ŚÖŠÉś³ÉµČĮæµÄI2Ź±×ŖŅʵē×ÓŹż±ČĪŖ1”Ć5 |
 æŖŠÄĶÜדŌŖ²āŹŌ¾ķĻµĮŠ“š°ø
æŖŠÄĶÜדŌŖ²āŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ÓĆøßĢśĖįÄĘ£ØNa2FeO4£©¶ŌŗÓĖ®”¢ŗžĖ®Ļū¶¾£¬ŹĒ³ĒŹŠŅūÓĆĖ®Ļū¶¾µÄŠĀ¼¼Źõ”£ŅŃÖŖÖʱøøßĢśĖįÄʵķ“Ó¦ĪŖFe2O3+3Na2O2=2Na2FeO4+Na2O£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
| A£®Na2O2¼ČŹĒŃõ»Æ¼Į£¬ÓÖŹĒ»¹Ō¼Į |
| B£®Fe2O3ŌŚ·“Ó¦ÖŠµĆµ½µē×Ó |
| C£®3 mol Na2O2²Ī¼Ó·“Ó¦,×ŖŅʵĵē×Ó×ÜŹżĪŖ12mol |
| D£®Na2FeO4ÄÜĻū¶¾É±¾ś£¬ŅņĘä¾ßÓŠĒæŃõ»ÆŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
³£ĪĀ£¬ĻĀĮŠĘųĢå²»Äܹ²“ęĒŅ·¢ÉśµÄ·“Ó¦ŹōÓŚ·ĒŃõ»Æ»¹ŌµÄŹĒ
| A£®NOŗĶO2 | B£®SO2ŗĶH2S |
| C£®NH3ŗĶHCl | D£®Cl2ŗĶSO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŅŃÖŖĻĀĮŠ·“Ó¦£ŗCo2O3 + 6HCl(ÅØ) = 2CoCl2 + Cl2”ü+ 3H2O £ØI£©
5Cl2 + I2 + 6H2O =" 10HCl" + 2HIO3 £ØII£©
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
| A£®·“Ó¦IÖŠHClŹĒŃõ»Æ¼Į |
| B£®·“Ó¦II ÖŠCl2·¢ÉśŃõ»Æ·“Ó¦ |
| C£®»¹ŌŠŌ£ŗCoCl2£¾ HCl £¾ I2 |
| D£®Ńõ»ÆŠŌ£ŗCo2O3£¾ Cl2£¾HIO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ijĻ”ĮņĖįŗĶĻ”ĻõĖįµÄ»ģŗĻČÜŅŗ200 mL£¬Ę½¾ł·Ö³ÉĮ½·Ż”£ĻņĘäÖŠŅ»·ŻÖŠÖš½„¼ÓČėĶ·Ū£¬×ī¶ąÄÜČܽā19.2 g”£ĻņĮķŅ»·ŻÖŠÖš½„¼ÓČėĢś·Ū£¬²śÉśĘųĢåµÄĮæĖęĢś·ŪÖŹĮæŌö¼ÓµÄ±ä»ÆČēĶ¼ĖłŹ¾”£ĻĀĮŠ·ÖĪö»ņ½į¹ū“ķĪóµÄŹĒ
A£®Ō»ģŗĻĖįÖŠ ĪļÖŹµÄĮæÅضČĪŖ2 mol/L ĪļÖŹµÄĮæÅضČĪŖ2 mol/L |
| B£®OA¶Ī²śÉśµÄŹĒNO£¬AB¶ĪµÄ·“Ó¦ĪŖFe£«2Fe3£«=3Fe2£«£¬BC¶Ī²śÉśĒāĘų |
| C£®µŚ¶ž·ŻČÜŅŗÖŠ×īÖÕČÜÖŹĪŖFeSO4 |
| D£®H2SO4ÅضČĪŖ2.5 mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
½«51£®2 g CuĶźČ«ČÜÓŚŹŹĮæÅØĻõĖįÖŠ£¬ŹÕ¼Æµ½µŖµÄŃõ»ÆĪļ(ŗ¬NO”¢N2O4”¢NO2)µÄ»ģŗĻĪļ¹²0£®8 mol£¬ÕāŠ©ĘųĢåĒ”ŗĆÄܱ»500 mL 2 mol/L NaOHČÜŅŗĶźČ«ĪüŹÕ£¬·¢ÉśµÄ·“Ó¦ĪŖ£ŗ2NO2£«2NaOH=NaNO2£«NaNO3£«H2O£»NO£«NO2£«2NaOH=2NaNO2£«H2O”£
ŌņÉś³ÉµÄŃĪČÜŅŗÖŠNaNO2µÄĪļÖŹµÄĮæĪŖ
| A£®0£®4 mol | B£®0£®6 mol |
| C£®0£®8 mol | D£®0£®2 mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
»š·ØĮ¶ĶŹ×ĻČŅŖ±ŗÉÕ»ĘĶæó£¬Ęä·“Ó¦ĪŖ2CuFeS2£«O2”Ŗ”śCu2S£«2FeS£«SO2ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
| A£®SO2¼ČŹĒŃõ»Æ²śĪļÓÖŹĒ»¹Ō²śĪļ |
| B£®CuFeS2½ö×÷»¹Ō¼Į£¬ĮņŌŖĖŲ±»Ńõ»Æ |
| C£®ĆæÉś³É1 mol Cu2S£¬ÓŠ4 molĮņ±»Ńõ»Æ |
| D£®Ćæ×ŖŅĘ1.2 molµē×Ó£¬ÓŠ0.2 molĮņ±»»¹Ō |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŠæÓėŗÜĻ”µÄĻõĖį·“Ӧɜ³ÉĻõĖįŠæ”¢ĻõĖįļ§ŗĶĖ®”£µ±Éś³É1 molĻõĖįŠæŹ±£¬±»»¹ŌµÄĻõĖįµÄĪļÖŹµÄĮæĪŖ (””””)”£
| A£®2 mol | B£®1 mol | C£®0.5 mol | D£®0.25 mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
½«11.9 gÓÉMg”¢Al”¢Fe×é³ÉµÄŗĻ½šČÜÓŚ×ćĮæµÄNaOHČÜŅŗÖŠ£¬ŗĻ½šÖŹĮæ¼õÉŁĮĖ2.7 g”£
ĮķČ”µČÖŹĮæµÄŗĻ½šČÜÓŚ¹żĮæĻ”ĻõĖįÖŠ£¬Éś³ÉĮĖ6.72 L NO(±ź×¼×“æöĻĀ)£¬Ļņ·“Ó¦ŗóµÄČÜŅŗÖŠ¼ÓČėŹŹĮæNaOHČÜŅŗĒ”ŗĆŹ¹Mg2£«”¢Al3£«”¢Fe3£«ĶźČ«×Ŗ»ÆĪŖ³Įµķ£¬Ōņ³ĮµķµÄÖŹĮæĪŖ(””””)
| A£®22.1 g | B£®27.2 g |
| C£®30 g | D£®ĪŽ·Ø¼ĘĖć |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com