
| 10-14 |
| 10-9 |
| 10-14 |
| 10-9 |
| V1 |
| V2 |
| 10-5 |
| 10-4 |


科目:高中化学 来源: 题型:
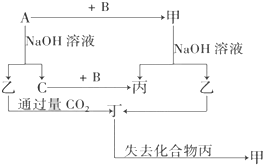 由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有如图示的转换关系,已知C为密度最小的气体,甲是电解质.
由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有如图示的转换关系,已知C为密度最小的气体,甲是电解质.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分解反应 | B、化合反应 |
| C、置换反应 | D、氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、增大压强,平衡不移动,说明(m+n)一定等于(p+q) |
| B、升高温度,A的转化率减小,说明正反应是吸热反应 |
| C、若增加B的量,平衡体系颜色加深,说明B必是气体物质 |
| D、若B是气体,增加A的量,A、B转化率都一定增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCO3在水中溶解度很小,所以CaCO3是弱电解质 |
| B、若某种电解质溶液中含有未电离的分子,则该电解质一定是弱电解质 |
| C、氯气和氨气的水溶液导电性都很好,所以它们是电解质 |
| D、SO3的水溶液可以导电,但它不是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、进行蒸发操作时,应加热至混合物中有大量晶体析出时停止加热,用余热蒸干 |
| B、进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C、进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 按如图所示装置进行实验,并回答下列问题:
按如图所示装置进行实验,并回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 定时间/小时 | 0 | 1 | 2 | 4 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA |
| B、2.8g乙烯中含有共价键的数目为0.5NA |
| C、标准状况下,11.2L苯中含有分子的数目为0.5NA |
| D、在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com