
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| KSP | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-23 |
| 实验编号 | 起始浓度/mol/L | 反应后溶液的pH | |
| c (HA) | c (NaOH) | ||
| ① | 0.10 | 0.10 | 9 |
| ② | X | 0.05 | 7 |
分析 (1)根据H2CO3、HCO3-和HSO3-的电离平衡常数确定酸性的强弱;
(2)因加入盐酸,醋酸的电离平衡逆向移动,则c(CH3COO-)减小,醋酸的电离程度减小,但温度不变,则醋酸电离平衡常数不变,加盐酸时c(H+)增大;
(3)由表格中的数据可知,溶度积越小的越易转化为沉淀;
(4)HA与NaOH恰好反应生成NaA时,溶液显碱性,说明HA为弱酸;根据物料守恒分析.
解答 解:(1)H2CO3、HCO3-和HSO3-的电离平衡常数分别是:4.30×10-7、5.61×10-11、1.02×10-7,所以酸性顺序是:H2CO3>HSO3->HCO3-,
故答案为:H2CO3>HSO3->HCO3-;
(2)因加入盐酸,醋酸的电离平衡逆向移动,则c(CH3COO-)减小,醋酸的电离程度减小,但温度不变,则醋酸电离平衡常数和水的离子积常数不变,加盐酸时c(H+)增大,
故答案为:AD;
(3)由表格中的数据可知,溶度积越小的越易转化为沉淀,显然只有硫化物的溶度积小,则应选择硫化钠,
故答案为:B;
(4)由实验①可知,HA与NaOH恰好反应生成NaA时,溶液显碱性,说明HA为弱酸,若要混合显中性,则HA要稍微过量,所以X大于0.05;实验①中溶液的溶质为NaA,由物料守恒可知,c(A-)+c(HA)=0.05 mol•L-1;
故答案为:大于;0.05 mol•L-1.
点评 本题考查了盐类水解、弱酸的电离平衡常数与酸性强弱的关系、弱酸的电离平衡的移动、沉淀的转化,题目难度中等,侧重于考查学生的分析能力和计算能力.


科目:高中化学 来源: 题型:选择题
| 物质(括号内为杂质) | 试剂 | |
| A | CO2(SO2) | Na2CO3溶液 |
| B | FeCl3溶液(CuCl2) | Fe |
| C | Fe2O3(Al2O3) | NaOH溶液 |
| D | Na2SO4溶液(Na2CO3) | 盐酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-甲基丁烷也称异丁烷 | |
| B. | 由乙烯生成乙醇属于加成反应 | |
| C. | C4H9Cl有3种同分异构体 | |
| D. | 光照条件下,甲烷通入氯水中,氯水黄绿色褪去,说明甲烷与氯水发生了取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuCl2溶液蒸干灼烧后得到CuCl2固体 | |
| B. | 火力发电的目的是使化学能转换为电能 | |
| C. | 已知C(石墨,s)=C(金刚石,s)△H>0,无法比较二者的稳定性. | |
| D. | 将FeCl3固体溶于适量蒸馏水来配制FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4与 Ba(OH)2 溶液反应:Ba2++SO42-+H++OH-═BaSO4↓+H2O | |
| B. | 金属钠与水的反应:Na+H2O═Na++OH-+H2↑ | |
| C. | 向足量NaHCO3溶液中滴人少量Ca(OH)2溶液:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| D. | 常温下,将氯气通人水中:Cl2+H2O═2H++2Cl-+ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热 | |
| B. | 分液操作时,静置分层后要先放出分液漏斗中下层液体,再倒出上层液体 | |
| C. | 分液操作时,选择的萃取剂的密度必须比水大 | |
| D. | 用胶头滴管向试管滴加液体时,滴管尖端靠在试管内壁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
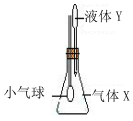 在如图所示示装置中,将液体Y滴入瓶中并摇动,一会儿小气球胀大.则气体X与液体Y可能是( )
在如图所示示装置中,将液体Y滴入瓶中并摇动,一会儿小气球胀大.则气体X与液体Y可能是( )| A | B | C | D | |
| 气体X | NH3 | SO2 | CO2 | HCl |
| 液体Y | 稀硫酸 | 浓NaOH | 饱和NaHCO3 | 水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑥ | B. | ②④⑤ | C. | ①②③④ | D. | ④⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com