

分析 (1)B中有电源是电解池,C为铜的电解精炼装置,为电解池;
(2)铜、锌原电池中,锌为负极,被氧化,铜为正极,发生还原反应;
(3)该装置是电解池,阳极上活泼金属,所以阳极上金属失电子发生氧化反应,正极上阴离子得电子发生还原反应,根据阴阳极上的电极反应式确定溶液浓度是否变化;
(4)B池中Pt棒为阳极,氯离子在阳极发生氧化反应生成氯气.
解答 解:解:(1)A没有外接电源,属于原电池,BC装置都有外接电源,所以是把电能转化为化学能的装置,属于电解池,故答案为:A;
(2)铜、锌、氯化铜原电池中,锌作负极,负极上锌失电子发生氧化反应,电极反应式为:Zn-2e-=Zn2+,
故答案为:负;
(3)铜的电解精炼装置中粗铜作阳极,精铜作阴极,阴极上铜离子得电子发生还原反应,电极反应式为:Cu2++2e-=Cu,粗铜是阳极,阳极上铜失电子发生氧化反应,电极反应式为:Cu-2e-=Cu2+,另外还原比铜活泼的Zn、Fe等失电子,阴极上析出的铜多于阳极上溶解的铜,所以溶液中CuCl2浓度减小,
故答案为:负;减小;
(4)B池中Pt棒为阳极,氯离子在阳极发生氧化反应生成氯气,电极反应式为2Cl--2e-=Cl2↑,故答案为:2Cl--2e-=Cl2↑.
点评 本题考查原电池和电解池原理,为高频考点,侧重于学生的分析能力的考查,注意把握原电池、电解池的原理,把握电极方程式的书写,难度不大.


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:选择题
| A. | 饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH增大 | |
| B. | AgCl悬浊液中存在平衡:AgCl(s)?Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小 | |
| C. | 为减小洗涤过程中固体的损失,最好选用稀H2SO4代替H2O来洗涤BaSO4沉淀 | |
| D. | 硬水中含有较多的Ca2+、Mg2+、HCO3-、SO42-,加热煮沸可以完全除去其中的 Ca2+、Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油的催化裂化是为了提高汽油等轻质油的产量和质量 | |
| B. | 石油裂解可得到汽油 | |
| C. | 煤的气化和液化均为物理变化 | |
| D. | 石油在分馏过程中最先得到的馏分是柴油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热的反应一定是吸热反应 | |
| B. | 化学反应就是旧化学键断裂、新化学键形成的过程 | |
| C. | 化学反应一定伴随着能量的变化 | |
| D. | 化石燃料并非在任何情况下都能充分燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙炔和苯 | B. | 甲醛与乙醛 | C. | 甲烷和乙酸 | D. | 丙烯和丁烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2+ (过氧乙酸)→ (过氧乙酸)→ +CH3COOH +CH3COOH | |
| B. | CH2=CH2+Cl2+Ca(OH)2→ +CaCl2+H2O +CaCl2+H2O | |
| C. |  $\stackrel{催化剂}{→}$ $\stackrel{催化剂}{→}$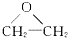 +HOCH2CH2-O-CH2CH2OH+2H2O +HOCH2CH2-O-CH2CH2OH+2H2O | |
| D. | 2CH2=CH2+O2$\stackrel{催化剂}{→}$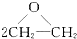 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com