

 进行此步操作时应关闭_________,打开_________ (填k1、k2或k3);
进行此步操作时应关闭_________,打开_________ (填k1、k2或k3);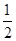 ×22.4=80.64ml
×22.4=80.64ml

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.0.045mol/L | B.0.036mol/L | C.0.026mol/L | D.0.028mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.20mL | B.25mL | C.28mL | D.33mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
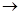 丙+丁
丙+丁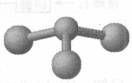
 ,此反应的化学方程式是 。
,此反应的化学方程式是 。 加到一定量丙
加到一定量丙
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1:1 | B.3:2 | C.2:1 | D.4:1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


 ③ 淀粉 ④ 白酒 ⑤ 食醋,进行实验,下列几组合适的是 (填序号)。
③ 淀粉 ④ 白酒 ⑤ 食醋,进行实验,下列几组合适的是 (填序号)。| A.③⑤ | B.①②④ |
| C.①②⑤ | D.①②③⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
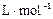 ,结果保留到小数点后三位)。
,结果保留到小数点后三位)。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com