
分析 题给物质都为强碱弱酸盐,水解呈碱性,相同物质的量浓度的盐溶液,溶液pH越大,则对应的酸的酸性越强,结合强弱与较弱酸的盐反应解答该题.
解答 解:(1)相同物质的量浓度的盐溶液,溶液pH越大,则对应的酸的酸性越强,由pHNaAlO2>Na2CO3>NaClO>NaHCO3>CH3COONa>NaNO2可知酸性HNO2>CH3COOH>H2CO3>HClO>HCO3->Al(OH)3,则酸性由强到弱的顺序是b、d、c、a,故答案为:b、d、c、a;
(2)CH3COONa为强碱弱酸盐,水解呈碱性,离子方程式为CH3COO-+H2O?CH3COOH+OH-,故答案为:CH3COO-+H2O?CH3COOH+OH-;
(3)因酸性H2CO3>HClO>HCO3-,则少量CO2通入NaClO溶液发生ClO-+CO2+H2O═HClO+HCO3-,通入NaAlO2溶液发生2AlO2-+3H2O+CO2═2Al(OH)3↓+CO32-,
故答案为:ClO-+CO2+H2O═HClO+HCO3-;2AlO2-+3H2O+CO2═2Al(OH)3↓+CO32-;
(4)NaHCO3为强碱弱酸盐,FeCl3为强酸弱碱盐,二者混合发生互促水解反应,反应的离子方程式是Fe3++3HCO3-═Fe(OH)3↓+3CO2↑,
故答案为:Fe3++3HCO3-═Fe(OH)3↓+3CO2↑.
点评 本题考查弱电解质的电离以及盐类水解等知识,为高频考点,题目难度中等,明确酸的强弱、酸根离子水解能力的关系是解本题关键,试题培养了学生的灵活应用能力.


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:解答题
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ②H2SO4 | ③NaOH ④Ba(OH)2 | ⑤Na2CO3 ⑥K2SO4 | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
如表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )| 选项 | a | b | c |
| A | Fe | FeCl3 | FeCl2 |
| B | HCl | Cl2 | HClO |
| C | H2SO4 | SO2 | SO3 |
| D | CH2=CH2 | CH3CH2OH | CH3CHO |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子最外层有3个电子的一种金属 | |
| B. | 熔点低于100℃的一种金属 | |
| C. | 次外电子层上有8个电子的一种元素 | |
| D. | 除最外层,原子的其他电子层电子数目均达饱和的一种金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
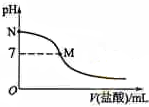 298K时,在20.0mL 0.10mol•L-1氨水中滴入0.10mol•L-的盐酸,溶液的pH与所加盐酸的体积关系如图所示.已知0.10mol•L-1氨水的电离度为1.32%,下列有关叙述正确的是( )
298K时,在20.0mL 0.10mol•L-1氨水中滴入0.10mol•L-的盐酸,溶液的pH与所加盐酸的体积关系如图所示.已知0.10mol•L-1氨水的电离度为1.32%,下列有关叙述正确的是( )| A. | 该滴定过程应该选择石蕊作为指示剂 | |
| B. | M点对应的盐酸体积为20.0 mL | |
| C. | M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-) | |
| D. | N点处的溶液中pH<12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化镁中滴加盐酸:H++OH-═H2O | |
| B. | 碳酸氢钙溶液与稀硝酸反应:Ca(HCO3)2+2H+=Ca2++CO2↑+H2O | |
| C. | 金属铝溶于氢氧化钠溶液:2Al+6OH-═2AlO2-+3H2↑ | |
| D. | 用FeCl3溶液腐蚀铜电路板:2Fe3++Cu═2Fe2++Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com