
ĻĀ±ķÖŠøł¾ŻŹµŃé²Ł×÷ŗĶĻÖĻóĖłµĆ³öµÄ½įĀŪÕżČ·µÄŹĒ
Ń”Ļī | ŹµŃé²Ł×÷ | ŹµŃéĻÖĻó | ½įĀŪ |
A | ijÄĘŃĪWÖŠ¼ÓČėĻ”ĮņĖį£¬²śÉśµÄĪŽÉ«ĪŽĪ¶µÄĘųĢåĶØČė³ĪĒåŹÆ»ŅĖ® | ŹÆ»ŅĖ®±ä»ė×Ē | WæÉÄÜŹĒNa2CO3 |
B | ÕŗÓŠÅØ°±Ė®µÄ²£Į§°ōææ½üČÜŅŗX | ÓŠ°×ŃĢ²śÉś | XŅ»¶ØŹĒÅØŃĪĖį |
C | ĒæĖįŠŌČÜŅŗYÖŠ¼ÓČėBa(NO3)2ČÜŅŗ£¬¾²ÖĆŗóŌŁ¼ÓČėKSCNČÜŅŗ | ĻČÓŠ°×É«³Įµķ£¬ ŗóČÜŅŗÓÖ±äŗģ | YÖŠŅ»¶Øŗ¬ÓŠSO42£ŗĶFe3+ |
D | ÉŁĮæĘųĢ¬Č²ĢžZĶØČėpH=aµÄäåĖ®ÖŠ | äåĖ®ĶŹÉ«£¬ČÜŅŗµÄpHČŌŌ¼ĪŖa | ZÓėäå·¢ÉśĮĖČ”“ś·“Ó¦ |
 Ļ°Ģā¾«Ń”ĻµĮŠ“š°ø
Ļ°Ģā¾«Ń”ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ѧğ½Ī÷Ź”¾°µĀÕņŹŠøßČżµŚŅ»“ĪÄ£Äāæ¼ŹŌ¾ķĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĪŖŌöĒæĀĮµÄÄĶøÆŹ“ŠŌ£¬ĻÖŅŌĒ¦Šīµē³ŲĪŖĶāµēŌ“£¬ŅŌA1×÷Ńō¼«”¢Pb×÷Ņõ¼«£¬µē½āĻ”ĮņĖį£¬Ź¹ĀĮ±ķĆęµÄŃõ»ÆĤŌöŗń”£·“Ó¦ŌĄķČēĻĀ£ŗµē³Ų£ŗPb(s)+ PbO2(s)+2H2SO4(aq)= 2PbSO4(s)+ 2H2O(l)
µē½ā³Ų£ŗ2Al + 3H2O  Al2O3 + 3H2”ü£¬µē½ā¹ż³ĢÖŠ£¬ŅŌĻĀÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©
Al2O3 + 3H2”ü£¬µē½ā¹ż³ĢÖŠ£¬ŅŌĻĀÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©
| Ōµē³Ų | µē½ā³Ų |
A | H+ŅĘĻņPbµē¼« | H+ŅĘĻņPbµē¼« |
B | ĆæĻūŗÄ3molPb | Éś³É2molAl2O3 |
C | Õż¼«£ŗPbO2+4H++2e-=Pb2++2H2O | Ńō¼«£ŗ2Al+3H2O-6e-=Al2O3+6H+ |
D |
|
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ѧğ½ĖÕŹ”øßȿğ¼¶Ä£Äāæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ŅŃÖŖX”¢Y”¢Z”¢W”¢KĪåÖÖŌŖĖŲ¾łĪ»ÓŚÖÜĘŚ±ķµÄĒ°ĖÄÖÜĘŚ£¬ĒŅŌ×ÓŠņŹżŅĄ“ĪŌö“ó”£ŌŖĖŲXŹĒÖÜĘŚ±ķÖŠŌ×Ó°ė¾¶×īŠ”µÄŌŖĖŲ£»YµÄ»łĢ¬Ō×ÓÖŠµē×ÓÕ¼¾ŻĮĖČżÖÖÄÜĮæ²»Ķ¬µÄŌ×Ó¹ģµĄ£¬ĒŅÕāČżÖÖ¹ģµĄÖŠµÄµē×ÓŹżĻąĶ¬£»WĪ»ÓŚµŚ2ÖÜĘŚ£¬ĘäŌ×ÓµÄŗĖĶā³É¶Ōµē×ÓŹżŹĒĪ“³É¶Ōµē×ÓŹżµÄ3±¶£»KĪ»ÓŚdsĒųĒŅŌ×ÓµÄ×īĶā²ćµē×ÓŹżÓėXµÄĻąĶ¬”£
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ£Ø“šĢāŹ±£¬X”¢Y”¢Z”¢W”¢KÓĆĖł¶ŌÓ¦µÄŌŖĖŲ·ūŗűķŹ¾£©
¢ÅY”¢Z”¢WŌŖĖŲµÄµŚŅ»µēĄėÄÜÓɓ󵽊”µÄĖ³ŠņŹĒ”” ”””£
¢ĘKµÄ¶ž¼ŪĄė×Óµē×ÓÅŲ¼Ź½ŹĒ”” ”””£
¢ĒY”¢ZŌŖĖŲµÄijŠ©Ēā»ÆĪļµÄ·Ö×ÓÖŠ¾łŗ¬ÓŠ18øöµē×Ó£¬ŌņYµÄÕāÖÖĒā»ÆĪļµÄ»ÆѧŹ½ŹĒ”” ””£»Y”¢ZµÄÕāŠ©Ēā»ÆĪļµÄ·ŠµćĻą²ī½Ļ“óµÄÖ÷ŅŖŌŅņŹĒ”” ”””£
¢ČČōX”¢Y”¢WŠĪ³ÉµÄij»ÆŗĻĪļ(Ļą¶Ō·Ö×ÓÖŹĮæĪŖ46)³ŹĖįŠŌ£¬ŌņøĆ»ÆŗĻĪļ·Ö×ÓÖŠYŌ×Ó¹ģµĄµÄŌÓ»ÆĄąŠĶŹĒ”” ””£»1 moløĆ·Ö×ÓÖŠŗ¬ÓŠ ¦Ņ¼üµÄŹżÄæŹĒ”” ”””£
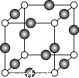
¢ÉZ”¢KĮ½ŌŖĖŲŠĪ³ÉµÄij»ÆŗĻĪļµÄ¾§°ū½į¹¹ČēĶ¼ĖłŹ¾£¬ŌņøĆ»ÆŗĻĪļµÄ»ÆѧŹ½ŹĒ”” ””£¬ZŌ×ÓµÄÅäĪ»ŹżŹĒ”” ”””£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ѧğ½ĖÕŹ”øßȿğ¼¶Ä£Äāæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
³£ĪĀĻĀ£¬ĻĀĮŠø÷×éĄė×ÓŌŚÖø¶ØČÜŅŗÖŠŅ»¶ØÄÜ“óĮæ¹²“ęµÄŹĒ
A£®ĪŽÉ«ČÜŅŗÖŠ£ŗK+”¢Na+”¢Cu2+”¢SO42£
B£®c(OH£)£½10£13 mol”¤L£1µÄČÜŅŗÖŠ£ŗAl3+”¢NO3£”¢I£”¢Cl£
C£®Ė®µēĄė²śÉśµÄc(H+)£½10£13 mol”¤L£1µÄČÜŅŗÖŠ£ŗNa+”¢Cl£”¢NO3£”¢SO42£
D£®0.1 mol”¤L£1FeSO4ČÜŅŗÖŠ£ŗK+”¢NH4+”¢MnO4£”¢ClO£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ѧğ½ĖÕŹ”ÄĻ¾©ŹŠ”¢ŃĪ³ĒŹŠøßČżµŚŅ»“ĪÄ£Äāæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
µžµŖ»ÆÄĘ£ØNaN3£©ŹĒĘū³µ°²Č«ĘųÄŅÖŠµÄÖ÷ŅŖ³É·Ö£¬ÄÜŌŚ·¢ÉśÅöײµÄĖ²¼ä·Ö½ā²śÉś“óĮæĘųĢ彫ĘųÄŅ¹ÄĘš”£ŹµŃéŹŅ²ā¶ØµžµŖ»ÆÄĘѳʷ֊NaN3µÄÖŹĮæ·ÖŹż”£ŹµŃé²½ÖčČēĻĀ£ŗ
¢Ł³ĘČ”Ō¼2.5000gµžµŖ»ÆÄĘŹŌŃł£¬Åä³É250mLČÜŅŗ”£
¢Ś×¼Č·ĮæČ”25.00mLČÜŅŗÖĆӌ׶ŠĪĘæÖŠ£¬ÓƵĪ¶Ø¹Ü¼ÓČė50.00mL 0.1000mol”¤L£1
(NH4)2Ce(NO3)6£ØĮłĻõĖįīęļ§£©£¬
[·¢Éś·“Ó¦ĪŖ£ŗ2(NH4)2Ce(NO3)6 +2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2”ü]£ØŌÓÖŹ²»²ĪÓė·“Ó¦£©”£
¢Ū·“Ó¦ŗó½«ČÜŅŗÉŌĻ”ŹĶ£¬Č»ŗóĻņČÜŅŗÖŠ¼ÓČė5mLÅØĮņĖį£¬µĪČė2µĪĮŚ·ĘßÜßųÖøŹ¾Ņŗ£¬ÓĆ0.0500mol”¤L£1(NH4)2Fe(SO4)2£ØĮņĖįŃĒĢśļ§£©±ź×¼µĪ¶ØČÜŅŗµĪ¶Ø¹żĮæµÄCe4+ÖĮČÜŅŗÓɵĀĢÉ«±äĪŖ»ĘŗģÉ«£Ø·¢ÉśµÄ·“Ó¦ĪŖ£ŗCe4++Fe2+= Ce3++Fe3+£©£¬ĻūŗÄĮņĖįŃĒĢśļ§±ź×¼ČÜŅŗ24.00mL”£
£Ø1£©²½Öč¢ŁÅäÖʵžµŖ»ÆÄĘČÜŅŗŹ±£¬³żŠčÓƵ½ÉÕ±”¢²£Į§°ō”¢ĮæĶ²Ķā£¬»¹ÓƵ½µÄ²£Į§ŅĒĘ÷ÓŠ ”¢ ”£
£Ø2£©µžµŖ»ÆÄĘŹÜײ»÷Ź±Éś³ÉĮ½ÖÖµ„ÖŹ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø3£©ČōĘäĖü¶ĮŹżÕżČ·£¬µĪ¶Øµ½ÖÕµćŗ󣬶ĮČ”µĪ¶Ø¹ÜÖŠ (NH4)2Fe(SO4)2±ź×¼ČÜŅŗĢå»ż°“Ķ¼Ķ¼Ź¾¶ĮČ”£¬½«µ¼ÖĀĖł²ā¶Øѳʷ֊µžµŖ»ÆÄĘÖŹĮæ·ÖŹż £ØŃ”Ģī£ŗ”°Ę«“ó”±”¢”°Ę«Š””±»ņ”°²»±ä”±£©”£
£Ø4£©Ķعż¼ĘĖćČ·¶ØµžµŖ»ÆÄĘŹŌŃłÖŠŗ¬NaN3µÄÖŹĮæ·ÖŹżĪŖ¶ąÉŁ£ØŠ“³ö¼ĘĖć¹ż³Ģ£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ѧğ½ĖÕŹ”ÄĻ¾©ŹŠ”¢ŃĪ³ĒŹŠøßČżµŚŅ»“ĪÄ£Äāæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ±ķŹ¾¶ŌÓ¦»Æѧ·“Ó¦µÄĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ
A£®ĀČĘųĶØČėĖ®ÖŠ£ŗCl2 + H2O  2H+ + Cl£+ClO£
2H+ + Cl£+ClO£
B£®ĒāŃõ»ÆĢś½ŗĢåÖŠ¼ÓČėHIČÜŅŗ£ŗFe(OH)3 + 3H+ = Fe3+ + 3H2O
C£®NaAlO2ČÜŅŗÖŠĶØČė¹żĮæCO2£ŗ2AlO2£+ CO2 + 3H2O = 2Al(OH)3”ż+ CO32£
D£®ÓĆĻ”ĻõĖį³żČ„ŹŌ¹ÜÄŚ±ŚŅų£ŗ3Ag+ 4H+ + NO3£ = 3Ag+ + NO”ü +2H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ѧğ½ĖÕŹ”ÄĻ¾©ŹŠ”¢ŃĪ³ĒŹŠøßČżµŚŅ»“ĪÄ£Äāæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
2013Äź10ŌĀŹĄ½ēĪĄÉś×éÖÆ°©Ö¢×ØĆÅ»ś¹¹Ź×“ĪÖøČĻ“óĘųĪŪČ¾”°¶ŌČĖĄąÖĀ°©”±”£ĻĀĮŠŠŠĪŖÓŠĄūÓŚ·ĄÖ¹“óĘųĪŪČ¾”¢¶ōÖĘĪķö²ĢģĘų·¢ÉśµÄŹĒ
A£®ŌŚĢļ¼ä·ŁÉÕ½ÕøĖ
B£®¶¬¼¾Č¼ÉÕ“óĮæŃĢĆŗ¹©ČČČ”ÅÆ
C£®Ģį³«æŖĖ½¼Ņ³µ³öŠŠ£¬¼õÉŁ³Ė×ų¹«½»³µ
D£®øÄÉĘÄÜŌ“½į¹¹£¬“óĮ¦·¢Õ¹Ģ«ŃōÄÜ”¢·ēÄܵČĒå½ąÄÜŌ“
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ѧğ¹ć¶«Ź”ĆÆĆūŹŠøßČżµŚ¶ž“Īøßæ¼Ä£ÄāĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŹŅĪĀĻĀ£¬0£®1mol”¤L£1CH3COONaČÜŅŗÓė 0£®1 mol”¤L£1NaClČÜŅŗµČĢå»ż»ģŗĻ£ØŗöĀŌČÜŅŗĢå»ż±ä»Æ£©£¬ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ
A£®»ģŗĻĒ°CH3COONaČÜŅŗÖŠÓÉĖ®µēĄė³öĄ“µÄc(OH”Ŗ)>1”Į10-7 mol”¤L-1
B£®»ģŗĻĒ°NaClČÜŅŗÖŠ£ŗc(Na+) + c(OH”Ŗ)= c(Cl£)+c(H+)
C£®»ģŗĻČÜŅŗÖŠ £ŗc(Cl£) >c(CH3COOH) >c(OH”Ŗ)
D£®»ģŗĻČÜŅŗÖŠ£ŗc(Cl£) + c(CH3COO£) =0£®1mol”¤L-1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ѧğ¹ć¶«Ź”ĒåŌ¶ŹŠøßČż4ŌĀÄ£ÄāĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠø÷×éĄė×ÓŌŚĶØČėSO2Ē°ŗó¾łÄÜ“óĮæ¹²“ęµÄŹĒ
A£®Ba2+”¢K+”¢Br£”¢Cl£ B£®Na+”¢Cu2+”¢OH£”¢SiO32£
C£®NH4+”¢Al3+”¢Br£”¢AlO2£ D£®Li+”¢H+”¢NO3£”¢SO42£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com