
已知25℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,向l00mL该条件下的CaSO4饱和溶液中加入400mL 0.0lmol·L-l的Na2SO4溶液,针对此过程的下列叙述正确的( )
A.溶液中析出CaSO4沉淀,最终溶液中c(SO42-)较原来大
B.溶液中无沉淀析出,溶液中c(Ca2+)、c (SO4-)都变小
C.溶液中析出CaSO4沉淀,溶液中c(Ca2+)、c(SO42-)都变小
D.溶液中无沉淀析出,但最终溶液中c(S042-)较原来大
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都同属于离子型碳化物,请通过CaC2制C2H2的反应进行思考,从中得到必要的启示,判断下列反应产物正确的是
A.ZnC2水解生成乙烷 B.Al4C3水解生成甲烷
C.Mg2C3水解生成丙烯 D.Li2C2水解生成乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
现有100mL混和溶液,其中H2SO4、HNO3和KNO3的物质的量浓度分别是6mol/L、2mol/L和1mol/L,向其中加入过量的铁粉,可产生标准状况下的混合气体体积为( )
A.11.2 L B.8.96 L C.6.72 L D.4.48 L
查看答案和解析>>
科目:高中化学 来源: 题型:
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一。下图是已经合成的最著名的硫-氮化合物的分子结构。下列说法正确的是( )
A.该物质的分子式为SN
B.该物质的分子中既有极性键又有非极性键
C.该物质可能是离子化合物
D.该物质的一个分子中含有9个N—S键
查看答案和解析>>
科目:高中化学 来源: 题型:
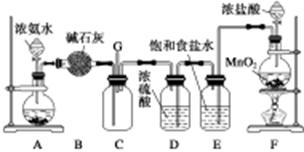 某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
请回答下列问题:
(1)装置F中发生反应的离子方程式为
_____________________________________
(2)NH3的结构式为
___________________________________
(3)E装置的作用
_____________________________________
(4)通入C装置的两根导管左边较长、右边较短,目的是_________________________
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式:____________________________________ ________
(6)该实验明显需要改进之处是_________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
运用化学反应原理分析解答以下问题
(1)已知: ①CO(g)+2H2(g)  CH3OH(g) △Hl= -91kJ·mol-l
CH3OH(g) △Hl= -91kJ·mol-l
②2CH3OH(g)  CH3OCH3(g)+H2O(g) △H2= -24 kJ·mol-l ③CO(g) +H2O(g)
CH3OCH3(g)+H2O(g) △H2= -24 kJ·mol-l ③CO(g) +H2O(g)  CO2(g)+H2(g) △H3= -1 kJ·mol-l
CO2(g)+H2(g) △H3= -1 kJ·mol-l
且三个反应的平衡常数依次为K1、K2、K3
则反应 3CO(g) +3H2(g)  CH3OCH3(g) +CO2(g) △H= .
CH3OCH3(g) +CO2(g) △H= .
化学平衡常数K= (用含K1、K2、K3的代数式表示)。
(2)一定条件下,若将体积比为1:2的CO和H2气体通入体积一定的密闭容器中发生反应
3CO(g) +3H2(g)  CH3OCH3(g) +CO2(g),下列能说明反应达到平衡状态是 。
CH3OCH3(g) +CO2(g),下列能说明反应达到平衡状态是 。
a.体系压强保持不变 b.混合气体密度保持不变
c. CO和H2的物质的量保持不变 d.CO的消耗速度等于CO2的生成速率
(3)氨气溶于水得到氨水。在25℃下,将x mol.L-l的氨水与y mol.L-1的盐酸等体积混合,反应后溶液中显中性,则c(NH4+)____c(Cl-)(填“>”、“<”、“=”);用含x和y的代数式表示出氨水的电离平衡常数 .
(4)科学家发明了使NH3直接用于燃料电池的方法,其装置用铂黑作电极、加入电解质溶液中,一个电极通入空气,另一电极通入NH3。其电池反应式为:4NH3+3O2  2N2+6H2O,电解质溶液应显 (填“酸性”、“中性”、“碱性”),
2N2+6H2O,电解质溶液应显 (填“酸性”、“中性”、“碱性”),
写出正极的电极反应方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Y元素形成的单质,常温下丙和己均为气体。已知反应:甲+乙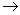 丁+己,甲+丙
丁+己,甲+丙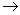 戊+己;常温下0.01 mol·L-1丁溶液的pH为12。下列说法正确的是
戊+己;常温下0.01 mol·L-1丁溶液的pH为12。下列说法正确的是
A.元素X在周期表中的位置为第2周期ⅥA族
B.元素X、Y、Z的原子半径由大到小的顺序为r(Z)>r(Y)>r(X)
C.1 mol甲与足量的乙完全反应转移的电子数为6.02×1023
D.1.0 L0.1 mol·L-1戊溶液中阴离子的总物质的量小于0.1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
水与人类文明的发展密切相关,下列说法正确的是
A.4 ℃时,纯水的pH=7
B.温度升高,纯水中的c(H+)增大,c(OH-)减小
C.水的电离程度很小,纯水中主要存在形态是水分子
D.向水中加入酸或碱,都可抑制水的电离,使水的离子积减小
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关钢铁腐蚀与防护的说法正确的是
A.钢管与电源正极连接,钢管可被保护
B.铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀
C.锌管与铜管露天堆放在一起,锌管不易被腐蚀
D.钢铁发生析氢腐蚀时,负极反应是Fe -3e-=Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com