
【题目】关于一定条件下的化学平衡H2(g)+I2(g)![]() 2HI(g) ΔH<0,下列说法正确的是( )
2HI(g) ΔH<0,下列说法正确的是( )
A.恒温恒容,充入H2,v(正)增大,平衡右移
B.恒温恒容,充入He,v(正)增大,平衡右移
C.加压,v(正),v(逆)不变,平衡不移动
D.升温,v(正)减小,v(逆)增大,平衡左移
 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
【题目】下列关于烃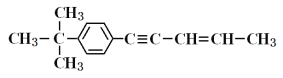 的说法正确的是
的说法正确的是
A. 共面的C原子最多为14个
B. 共直线的C原子只有为4个
C. 1mol该烃最多可以和6molH2发生加成反应
D. 1mol该烃最多可以消耗6molBr2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸亚铁是白色难溶于水的固铁剂。某小组利用如图装置,向装置③中通入CO2至溶液pH=7,然后滴入FeSO4溶液,过滤、洗涤、干燥制得FeCO3。
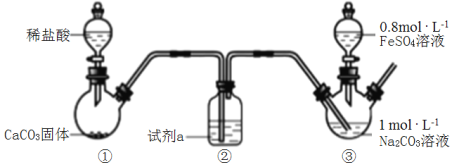
下列说法错误的是( )
A.试剂a是饱和NaHCO3溶液
B.碳酸钠溶液通入CO2至pH=7的目的是降低c(OH-),防止生成Fe(OH)2
C.装置③中生成沉淀的离子方程式为Fe2++CO![]() =FeCO3↓
=FeCO3↓
D.碳酸钠溶液显碱性的原因是CO![]() +H2OHCO
+H2OHCO![]() +OH-
+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知分解1mol H2O2放出热量98kJ,在含少量I-的溶液中,H2O2分解的机理为:
H2O2+I-→H2O+IO- 慢
H2O2+IO-→H2O+O2+I- 快
下列有关该反应的说法正确的是( )
A.反应速率与I-浓度无关
B.IO-也是该反应的催化剂
C.分解2mol H2O2放出热量196kJ
D.v(H2O2)=v(H2O)=v(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸阿比多尔是一种盐酸盐,其主要作用是通过抑制流感病毒脂膜与宿主细胞的融合而阻断病毒的复制,结构如图。回答下列问题:
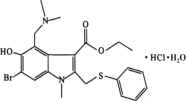
(1)盐酸阿比多尔中所含N、O、S三种元素第一电离能由大到小的顺序为___。O原子核外有___种不同运动状态的电子,基态S原子的价电子排布图不是![]() ,是因为该排布方式违背了___。
,是因为该排布方式违背了___。
(2)该结构中N原子的杂化方式是___。已知在氨分子中,H—N—H键角为107.3°,但是在[Zn(NH3)6]2+离子中H—N—H键角变为109.5°,分析原因为___。
(3)盐酸阿比多尔中不含有的化学键类型为___(填选项字母)。
A.离子键 B.配位键 C.金属键 D.σ键 E.π键 F.极性键 G.非极性键
(4)以氮化镓(GaN)为代表的第三代半导体材料目前已成为全球半导体研究的前沿和热点。GaN晶胞如图1所示,图2为晶胞沿y轴的投影1∶1平面图。
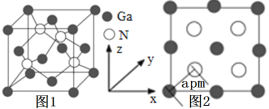
①氮化硼与氮化镓的结构类似,氮化硼熔点3000℃,氮化镓熔点1700℃,分析它们熔点不同的原因____。
②晶胞中与一个Ga原子距离最近且相等的N原子有____个。
③设阿伏加德罗常数的值为NA,则该晶胞的密度是___g·cm3(列出计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尼洛替尼用于治疗白血病有显著疗效。有机化合物M(![]() )是合成尼洛替尼的中间体,其一种合成路线如图:
)是合成尼洛替尼的中间体,其一种合成路线如图:

已知:含有α—氢的酯在醇钠等碱性缩合剂作用下发生缩合作用,失去一分子醇得到β—酮酸酯。如:
2CH3COOC2H5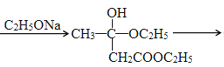 CH3COCH2COOC2H5+C2H5OH
CH3COCH2COOC2H5+C2H5OH
回答下列问题:
(1)有机物A中含氧官能团的名称为___。
(2)M的分子中最多有___个碳原子在同一个平面上,M存在顺反异构现象,其反式异构体的结构简式是___。
(3)反应①的化学方程式为___;其反应类型为___。
(4)有机物![]() 有多种同分异构体,其中含有苯环的硝基化合物有___种,写出其中一种具有手性碳的同分异构体的结构简式为___。
有多种同分异构体,其中含有苯环的硝基化合物有___种,写出其中一种具有手性碳的同分异构体的结构简式为___。
(5)写出以乙醇、乙酸、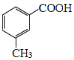 为原料合成
为原料合成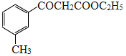 的合成路线(其它试剂任选)___。
的合成路线(其它试剂任选)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.1 mol·L-1NaOH溶液分别滴定20.00mL 0.1 mol·L-1的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是

A.Ⅰ、Ⅱ分别表示盐酸和醋酸的滴定曲线
B.pH=7时,滴定盐酸和醋酸消耗NaOH溶液的体积相等
C.V(NaOH)=10.00mL时,醋酸溶液中c(CH3COO-)> c(Na+)> c(H+)> c(OH-)
D.V(NaOH)=20.00mL时,两溶液中c(CH3COO-)> c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:H2S:Ka1=1.3×10-7 Ka2=7.1×10-16 ,H2CO3:Ka1=4.3×10-7 Ka2=5.6×10-11, CH3COOH:Ka=1.8×10-5,HClO2:Ka=1.1×10-2,NH3·H2O:Kb=1.8×10-5。
(1)①常温下,0.1 mol·L-1Na2S溶液和0.1 mol·L-1Na2CO3溶液,碱性更强的是_____,其原因是_______。
②25 ℃时,CH3COONH4溶液显__性。NaHCO3溶液的pH___CH3COONa溶液的pH。
③NH4HCO3溶液显__性,原因是_________。
(2)能证明Na2SO3溶液中存在SO32-+H2OHSO3—+OH-水解平衡的事实是___。
A.滴入酚酞溶液变红,再加H2SO4溶液红色褪去
B.滴入酚酞溶液变红,再加BaCl2溶液后产生沉淀且红色褪去
C.滴入酚酞溶液变红,再加氯水后红色褪去
(3)25 ℃时,浓度均为0.1 mol·L-1的NaClO2溶液和CH3COONa溶液,两溶液中c(ClO2—)___c(CH3COO-)。若要使两溶液的pH相等应___。
a.向NaClO2溶液中加适量水 b.向NaClO2溶液中加适量NaOH
c.向CH3COONa溶液中加CH3COONa固体 d.向CH3COONa溶液中加适量的水
(4)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是_______(用化学方程式表示)。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是 ________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛酸锰(MnTiO3)纳米材料是一种多用途催化剂。工业上用红钛锰矿(主要成分有MnTiO3,还含有少量FeO、Fe2O3、SiO2等杂质)来制备MnTiO3,其工艺流程如图所示:
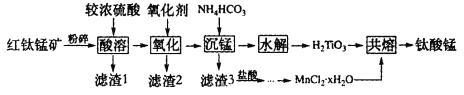
已知①红钛锰矿“酸溶”后Ti元素主要以TiO2+的形式存在;
②H2TiO3不溶于无机酸和碱,不溶于水;
③在空气中加热无水MnCl2分解放出HCl,生成Mn3O4。
回答下列问题:
(1)“粉碎”的目的是__。
(2)“酸溶”中发生的主要反应化学方程式为__。
(3)为了更好地把滤渣2分离出来,除搅拌外,还需要(填操作名称)___。
(4)“氧化”的氧化剂选用的是高锰酸钾,而不选择通常人们认可的绿色氧化剂“双氧水”,除了高锰酸钾氧化性强、反应快之外,还可能的原因是__(写出一条即可)。
(5)“沉锰”的条件一般控制在45℃以下的原因是__。
(6)TiO2+的水解率受温度和H+浓度的影响如图所示,TiO2+最适宜的水解条件是__。
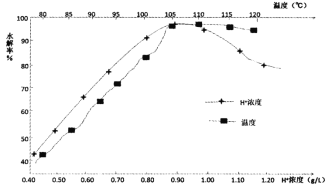
(7)测定所得MnCl2·xH2O晶体中结晶水的含量。取29.70g样品加热分解,热重曲线(TG)如图所示。
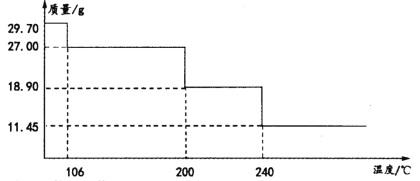
所得氯化锰晶体x的值是__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com