
【题目】有4种钠的化合物W、X、Y、Z,它们之间存在如下关系:
① W![]() X + H2O + CO2↑
X + H2O + CO2↑
② Z + CO2 → X + O2
③ Z + H2O → Y + O2↑
④ X + Ca(OH)2 → Y+ CaCO3↓
试回答下列问题:
(1)W、X、Y、Z的化学式分别是:W_____________,X_____________,Y_____________,Z_____________。
(2)以上4个化学反应,属于氧化还原反应的是__________________________(填反应序号)。在反应③中氧化剂是___________________(写化学式),还原剂是_____________(写化学式),写出反应②化学方程式并双线桥法标出电子转移方向、数目_______________________________________。
(3)若④反应在溶液中进行,写出其离子方程式__________________________。
【答案】NaHCO3 Na2CO3 NaOH Na2O2 ②③ Na2O2 Na2O2  CO32-+Ca2+=CaCO3↓
CO32-+Ca2+=CaCO3↓
【解析】
根据框图所示的内容,钠的化合物中,受热能分解生成三种产物的是碳酸氢钠,所以W是碳酸氢钠,碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,所以X是碳酸钠,能和二氧化碳以及水反应生成氧气的是过氧化钠,所以Z是过氧化钠,以此解答。
(1)根据框图所示的内容,钠的化合物中,受热能分解生成三种产物的是碳酸氢钠,所以W是碳酸氢钠,碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,所以X是碳酸钠,能和二氧化碳以及水反应生成氧气的是过氧化钠,所以Z是过氧化钠,故答案为:NaHCO3;Na2CO3;NaOH;Na2O2;
(2)以上4个化学反应中,反应2Na2O2+2CO2=2Na2CO3+O2↑和2Na2O2+2H20=4NaOH+O2↑中有元素化合价的变化,属于氧化还原反应,两个反应中化合价变化的均是过氧化钠中的氧元素,所以过氧化钠既是氧化剂又是还原剂,②化学方程式并双线桥法标出电子转移方向、数目为: ,故答案为:②③;Na2O2;Na2O2;
,故答案为:②③;Na2O2;Na2O2; 。
。
(3)碳酸钠和氢氧化钙反应的离子方程式为:CO32-+Ca2+=CaCO3↓故答案为:CO32-+Ca2+=CaCO3↓。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用NaI溶液中通入少量Cl2得到含碘废液,再利用含碘废液获取NaI固体,实验流程如下:

已知反应②:2I﹣+2Cu2++![]() +H2O
+H2O![]() 2CuI↓+
2CuI↓+![]() +2H+。
+2H+。
回答下列问题:
(1)过滤实验所需要的玻璃仪器有普通漏斗、烧杯、_____________。
(2)反应③中CuI被氧化,还原产物只有NO2,该反应的化学方程式为_________________。当有95.5 g CuI参与反应,则需要标况下______________L的O2才能将生成的NO2在水中完全转化为硝酸。
(3)化合物B中含两种元素,铁原子与另一种元素原子的物质的量之比为3∶8,则化合物B的化学式为_____________。
(4)反应⑤中生成黑色固体和无色气体,黑色固体的俗称为磁性氧化铁,则反应⑤的化学方程式为______。
(5)将足量的Cl2通入含12 g NaI的溶液中,一段时间后把溶液蒸干得到固体的质量为_________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚维酮碘的水溶液是一种常用的碘伏类缓释消毒剂,聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如图 ,下列说法不正确的是( )
,下列说法不正确的是( )
A.聚维酮的单体是![]() B.聚维酮分子由(m+n)个单体聚合而成
B.聚维酮分子由(m+n)个单体聚合而成
C.聚维酮碘是一种水溶性物质D.聚维酮在一定条件下能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家利用太阳能分解水生成的氢气在催化剂作用下与CO2反应生成甲醇。已知:H2(g)、CO(g)和CH3OH(l)的燃烧热ΔH分别为285.8kJ·mol1、283.0kJ·mol1和726.5kJ·mol1。
请回答下列问题:
(1)用太阳能分解10mol水消耗的能量是______kJ。
(2)写出表示H2(g)、CO(g)和CH3OH(l)燃烧热的热化学方程式。
①H2:__________;
②CO:__________;
③CH3OH:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请结合题中数据,写出对应的热化学方程式。
(1)16gCH3OH(l)与适量O2反应,生成CO2(g)和H2O(l),放出683.4kJ热量_____。
(2)N2(g)和H2(g)反应生成2 molNH3(g),放出92.2kJ热量_____。
(3)稀溶液中,1molH2SO4与NaOH完全反应时,放出114.6kJ热量,写出表示中和热的热化学方程式_______。
(4)agC(s)与足量O2反应生成CO2气体时,放出bkJ热量____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN,Al和N的相对原子质量分别为27和14)广泛用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应Al2O3+N2+3C![]() 2AlN+3CO合成。下列叙述正确的是( )
2AlN+3CO合成。下列叙述正确的是( )
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1mol AlN需转移3mol电子
C.AlN中氮元素的化合价为+3
D.AlN的摩尔质量为41g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的原电池,下列叙述正确的是(盐桥中装有含琼胶的KCl饱和溶液)( )
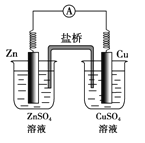
A. 反应中,盐桥中的K+会移向CuSO4溶液
B. 取出盐桥后,电流计依然发生偏转
C. 铜片上有气泡逸出
D. 反应前后铜片质量不改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某条件下N2与H2反应过程中能量变化的曲线图.根据图象判断下列叙述中正确的是( )
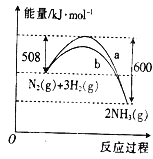
A. 该反应的热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) △H=+92kJ·mol﹣1
2NH3(g) △H=+92kJ·mol﹣1
B. a曲线是加入催化剂时的能量变化曲线
C. 加入催化剂,该化学反应的反应热数值会减小
D. 反应2NH3(g)![]() N2(g)+3H2(g)△H=+92kJ·mol﹣1
N2(g)+3H2(g)△H=+92kJ·mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容的密闭体系中,可逆反应:A(s)+2B(g)![]() 2C(g) ΔH<0,不能作为该反应达到化学平衡的标志的是
2C(g) ΔH<0,不能作为该反应达到化学平衡的标志的是
①v正(B)=v逆(C) ②n(B)∶n(C)=1∶1 ③容器内压强不再改变
④容器内气体的密度不再改变 ⑤容器内混合气体的平均相对分子质量不再改变
A. ②③④⑤ B. ①③④ C. ②③ D. 全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com