
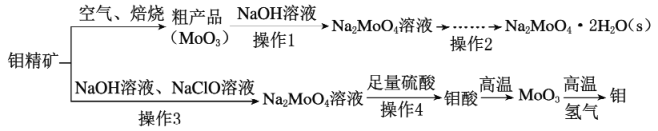
【题目】钼酸钠(Na2MoO4)是一种冷却水系统的金属缓蚀剂,工业上利用钼精矿(主要成分为MoS2)制备金属钼和钼酸钠晶体的流程如下图所示。
回答下列问题:
(1)如果在空气中焙烧1mol MoS2时,S转移12mol电子,则MoS2中钼元素的化合价为_________;焙烧的产物除MoO3外的另一种是_________,产生的尾气对环境的主要危害是____________________________。
(2)若在实验室中进行操作2,则从钼酸钠溶液中得到钼酸钠晶体的操作步骤是____________________,过滤、洗涤、干燥。
(3)钼精矿中MoS2含量的测定:取钼精矿16g,经在空气中焙烧、操作1、操作2得到钼酸钠晶体(Na2MoO4·2H2O)12.1g,钼精矿中MoS2的质量分数为_________________________。(已知MoS2的相对分子质量为160,Na2MoO4·2H2O的相对分子质量为242)。
(4)操作3发生反应的离子方程式为__________________________________________________。
(5)用镍、钼作电极电解浓NaOH溶液制备钼酸钠(Na2MoO4)的装置如图甲所示。b电极的材料为_______(填“镍”或“钼”),其电极反应式为_________________________________________________。
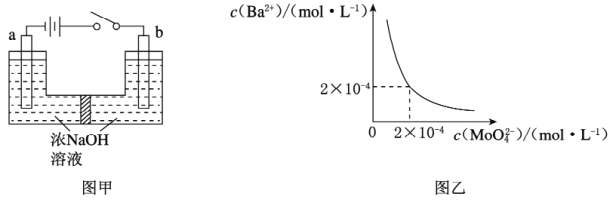
(6)某温度下,BaMoO4在水中的沉淀溶解平衡曲线如图乙所示,该温度下BaMoO4的Ksp为____________。
【答案】+4 SO2 形成酸雨 加热浓缩(或蒸发浓缩)、冷却结晶 50% MoS2 + 6OH- + 9ClO- =MoO42— + 2SO42— + 9Cl— + 3H2O 钼 Mo - 6e- + 8OH— = MoO42— + 4H2O 4×10-8
【解析】
灼烧钼精矿,MoS2燃烧,反应方程式为2MoS2+7O2 ![]() 2MoO3+4SO2,碱性条件下,MoO3和NaOH溶液反应,反应方程式为MoO3+2OH-=MoO42-+H2O,操作1是过滤,溶液中的溶质为Na2MoO4,操作2是将溶液蒸发浓缩、冷却结晶,然后重结晶得到Na2MoO4.2H2O;钼精矿,碱溶并用NaClO氧化,操作3,过滤也得到Na2MoO4与足量硫酸反应生成钼酸,高温灼烧钼酸生成MoO3,氢气还原MoO3得到Mo。
2MoO3+4SO2,碱性条件下,MoO3和NaOH溶液反应,反应方程式为MoO3+2OH-=MoO42-+H2O,操作1是过滤,溶液中的溶质为Na2MoO4,操作2是将溶液蒸发浓缩、冷却结晶,然后重结晶得到Na2MoO4.2H2O;钼精矿,碱溶并用NaClO氧化,操作3,过滤也得到Na2MoO4与足量硫酸反应生成钼酸,高温灼烧钼酸生成MoO3,氢气还原MoO3得到Mo。
(1)如果在空气中焙烧1mol MoS2时,S转移12mol电子,根据电子守恒:(+4-x)×2=12,x=-2,则MoS2中硫元素为-2价,钼元素的化合价为+4;焙烧的产物除MoO3外的另一种是SO2,产生的尾气对环境的主要危害是形成酸雨。故答案为:+4;SO2;形成酸雨;
(2)在实验室中进行操作2,从钼酸钠溶液中得到钼酸钠晶体的操作步骤是加热浓缩(或蒸发浓缩)、冷却结晶,过滤、洗涤、干燥。故答案为:加热浓缩(或蒸发浓缩)、冷却结晶;
(3)由关系式
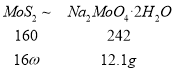
160:16ω=242:12.1g,ω=0.5,钼精矿中MoS2的质量分数为50%。故答案为:50%;
(4)操作3在碱性条件下,NaClO将MoS2 氧化生成MoO42— 和SO42—,发生反应的离子方程式为MoS2 + 6OH- + 9ClO- =MoO42— + 2SO42— + 9Cl— + 3H2O。故答案为:MoS2 + 6OH- + 9ClO- =MoO42— + 2SO42— + 9Cl— + 3H2O;
(5)b与电源正极相连,为阳极,b电极的材料为钼发生氧化反应,其电极反应式为Mo - 6e- + 8OH— = MoO42— + 4H2O。故答案为:钼;Mo - 6e- + 8OH— = MoO42— + 4H2O;
(6)由图乙:某温度下,BaMoO4的Ksp为c(Ba2+)c(MoO42-)==2×10-4×2×10-4= 4×10-8。故答案为:4×10-8。


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】已知A为常见的金属单质,各物质有如图所示的关系:
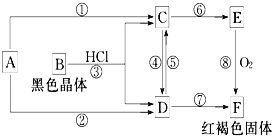
(1)写出B、C的化学式:
B:___,C:___,E:___,F___
(2)写出以下反应的化学方程式,有离子方程式的写离子方程式。
④___;⑤___;⑧___;颜色变化__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NOx、CO、SO2等大气污染气体的治理,对保护环境有重要的意义。回答下列问题:
(1)NOx与CO反应生成无污染气体的相关热化学方程式如下:
①NO2(g)+CO(g)![]() CO2(g)+NO(g) ΔH1=234.0kJ·mol1
CO2(g)+NO(g) ΔH1=234.0kJ·mol1
②4NO(g)![]() 2NO2(g)+N2(g) ΔH2=291.8kJ·mol1
2NO2(g)+N2(g) ΔH2=291.8kJ·mol1
反应③2NO2(g)+4CO(g)![]() N2(g)+4CO2(g)的ΔH3=___kJ·mol1,有利于提高该反应NO2平衡转化率的条件是___(填标号)。
N2(g)+4CO2(g)的ΔH3=___kJ·mol1,有利于提高该反应NO2平衡转化率的条件是___(填标号)。
A.高温低压 B.低温高压 C.高温高压 D.低温低压
(2)在一定温度下,向2L的恒容密闭容器中充入4.0molNO2和4.0molCO,在催化剂作用下发生反应:2NO2(g)+4CO(g)![]() N2(g)+4CO2(g),测得相关数据如下:
N2(g)+4CO2(g),测得相关数据如下:
0min | 5min | 10min | 15min | 20min | |
c(NO2)/mol·L1 | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
c(N2)/mol·L1 | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
①其他条件不变,若不使用催化剂,则0~5minNO2的转化率将___(填“变大”、“变小”或“不变”)。
②以下表述能说明该反应已达到平衡状态的是___。
A.CO的反应速率为N2的4倍
B.气体的颜色不再变化
C.化学平衡常数K不再变化
D.混合气的压强不再变化
③该温度下反应的化学平衡常数K=__(保留两位有效数字)。
④在20min时,保持温度不变,继续向容器中再加入2.0molNO2和2.0molN2,则化学平衡__移动(填“正向”、“逆向”或“不”)。
(3)在高效催化剂的作用下用CH4还原NO2,也可消除氮氧化物的污染。
①CH4还原NO2反应的化学方程式为___。
②在相同条件下,选用A、B、C三种不同催化剂进行反应,生成N2的物质的量与时间变化如图图1所示,其中活化能最大的是___[Ea(A)、Ea(B)、Ea(C)分别表示三种催化剂下该反应的活化能]。
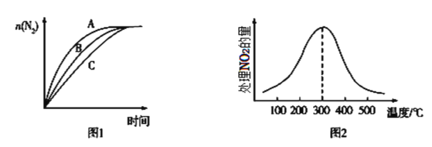
③在催化剂A作用下,测得相同时间内处理NO2的量与温度的关系如图2所示,曲线先增大后减小的可能原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
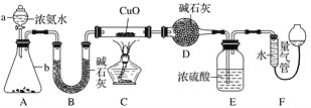
(1)仪器a的名称为______;仪器b中可选择的试剂为______。
(2)实验室中,利用装置A,还可制取的无色气体是______(填字母)。
A.Cl2 B.O2 C.CO2 D.NO2
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,上述现象证明NH3具有______性,写出相应的化学方程式______。
(4)E装置中浓硫酸的作用______。
(5)读取气体体积前,应对装置F进行的操作:______。
(6)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为n L(已折算成标准状况),则氨分子中氮、氢的原子个数比为______(用含m、n字母的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加罗常数的值,下列说法正确的是( )
A.标准状况下,22.4 L H2O中含有氢原子数目为2NA
B.17 g NH3所含质子数为10NA
C.0.1 mol Cu(NO3)2中含有的离子数目为0.2NA
D.28 g N2体积为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型镁-锂双离子二次电池如图,下列关于该电池的说法不正确的是( )
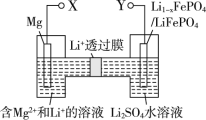
A.放电时,Li+由左向右移动
B.放电时,导线上每通过1 mol e-,左室溶液质量减轻5 g
C.充电时,外加电源的正极与Y相连
D.充电时,阳极上的电极反应式为LiFePO4 -xe-=Li1-xFePO4+xLi+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中一定量混合气体发生反应:2A(g)+B(g)![]() xC(g),达到平衡时测得A的浓度为0.5mol/L,在温度不变的条件下,将容器中的容积扩大到原来2倍,再达平衡时,测得A的浓度为0.3mol/L,下列有关判断正确的是
xC(g),达到平衡时测得A的浓度为0.5mol/L,在温度不变的条件下,将容器中的容积扩大到原来2倍,再达平衡时,测得A的浓度为0.3mol/L,下列有关判断正确的是
A. x=3 B. 平衡向正反应方向移动
C. B的转化率降低 D. C的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁用于照明弹,是因为镁能在空气中燃烧产生耀眼光芒,并发生如下三个反应:
①2Mg+O2![]() 2MgO、②3Mg+N2
2MgO、②3Mg+N2![]() Mg3N2、③2Mg+CO2
Mg3N2、③2Mg+CO2![]() 2MgO+C(黑色)。
2MgO+C(黑色)。
关于上述三个反应的叙述不正确的是( )
A.反应①②③的还原剂都是金属镁B.反应①和③中都是氧元素被还原
C.反应②的生成物中氮元素为-3价D.反应③的氧化剂是二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 [实验化学]
3,4亚甲二氧基苯甲酸是一种用途广泛的有机合成中间体,微溶于水,实验室可用KMnO4氧化3,4亚甲二氧基苯甲醛制备,其反应方程式为
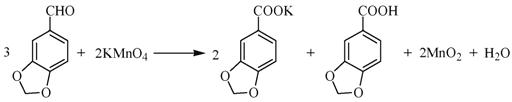
实验步骤如下:
步骤1:向反应瓶中加入3,4亚甲二氧基苯甲醛和水,快速搅拌,于70~80 ℃滴加KMnO4溶液。反应结束后,加入KOH溶液至碱性。
步骤2:趁热过滤,洗涤滤饼,合并滤液和洗涤液。
步骤3:对合并后的溶液进行处理。
步骤4:抽滤,洗涤,干燥,得3,4亚甲二氧基苯甲酸固体。
(1)步骤1中,反应结束后,若观察到反应液呈紫红色,需向溶液中滴加NaHSO3溶液,![]() 转化为_____________(填化学式);加入KOH溶液至碱性的目的是____________________________。
转化为_____________(填化学式);加入KOH溶液至碱性的目的是____________________________。
(2)步骤2中,趁热过滤除去的物质是__________________(填化学式)。
(3)步骤3中,处理合并后溶液的实验操作为__________________。
(4)步骤4中,抽滤所用的装置包括_______________、吸滤瓶、安全瓶和抽气泵。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com