
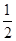 H2SO4(浓)+ NaOH(aq)=
H2SO4(浓)+ NaOH(aq)=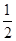 Na2SO4(aq)+ H2O(l) △H2 = m,下列说法正确的是( )
Na2SO4(aq)+ H2O(l) △H2 = m,下列说法正确的是( )| A.上述热化学方程式中的计量数表示分子个数 | B.△H1>△H2 |
| C.△H2 =" -" 57.3 kJ·mol-1 | D.|△H1|>|△H2| |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.降低温度,可提高b路线中乙醇的转化率 |
| B.从能量消耗的角度来看,b路线制氢更加有利 |
| C.乙醇可通过淀粉等生物原料发酵制得,属于可再生资源 |
| D.由a、b知:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 FeO(s)+CO(g) △H1=" a" kJ·mol-1
FeO(s)+CO(g) △H1=" a" kJ·mol-1 2CO2(g) △H2=" b" kJ·mol-1
2CO2(g) △H2=" b" kJ·mol-1 2FeO(s) △H3
2FeO(s) △H3| A.缩小反应器体积 | B.再通入CO2 |
| C.升高温度 | D.使用合适的催化剂 |
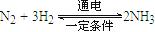 。则在电解法合成氨的过程中,应将H2不断地通入 极(填“正”、“负”、 “阴” 或“阳”);在另一电极通入N2,该电极反应式为 。
。则在电解法合成氨的过程中,应将H2不断地通入 极(填“正”、“负”、 “阴” 或“阳”);在另一电极通入N2,该电极反应式为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.C(固)+O2(气)=CO2(气); △H ="+393.5" kJ/mol |
B.C(固)+ O2(气)=CO(气); △H ="-393.5" kJ/mol O2(气)=CO(气); △H ="-393.5" kJ/mol |
| C.C + O2= CO2;△H ="-393.5" kJ/mol |
| D.C(固)+O2(气)=CO2(气); △H ="-393.5" kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.白磷在氧气中燃烧的热化学方程式是:P4(s)+5O2(g)=P4O10(s) ΔH=-745.8kJ·mol-1 |
| B.红磷转化成白磷时放出热量 |
| C.31g红磷中蕴含的能量为738.5k |
| D.红磷比白磷稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2A ( l ) + B ( l ) =" 2C" (g )△H1 | B.2A ( g ) + B ( g ) =" 2C" (g )△H2 |
| C.2A ( g ) + B ( g ) =" 2C" ( l )△H3 | D.2A ( l ) + B ( l ) =" 2C" ( l )△H4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
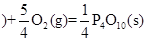 △H = —738.5kJ?mol-1
△H = —738.5kJ?mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com