
| A. | 标准状况下,22.4LH2O所含有原子数为3NA | |
| B. | 1mol OH-中含电子数目为9NA | |
| C. | 标准状况下,11.2LN2和NO的混合气体所含的原子数为NA | |
| D. | 每燃烧12gC,转移的电子数目为4NA |
分析 A.气体摩尔体积使用对象为气体;
B.1个氢氧根离子含有10个电子;
C.气体摩尔体积使用对象为气体,可以是单一气体,也可以是混合气体,氮气与一氧化氮都是双原子分子;
D.碳完全燃烧生成二氧化碳,不完全燃烧生成一氧化碳;
解答 解:A.标况下水是液体,不能使用气体摩尔体积,故A错误;
B.1mol OH-中含电子数目为10NA,故B错误;
C.氮气与一氧化氮都是双原子分子,标准状况下,11.2LN2和NO的混合气体物质的量为;$\frac{11.5L}{22.4L/mol}$=0.5mol,所含的原子数为0.5mol×2×NA=2NA,故C正确;
D.碳燃烧产物未知无法计算转移电子数,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数及相关计算,熟悉以物质的量为核心的计算公式,明确气体摩尔体积使用条件和对象是解题关键,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 增加溶液pH | B. | 加入2.0 mol/L NH4Cl | ||
| C. | 加入0.1 mol/L MgSO4 | D. | 加入适量95%乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与醋酸反应:Fe+2H+═Fe2++H2↑ | |
| B. | 硫酸铜溶液与氢氢化钡溶液混合:Ba2++SO42-═BaSO4↓ | |
| C. | 铜与硝酸银溶液反应:Cu+Ag+═Cu2++Ag | |
| D. | 碳酸氢钙与盐酸反应:HCO3-+H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 200mL 2mol/L MgCl2溶液 | B. | 1000mL 2.5mol/L NaCl溶液 | ||
| C. | 300mL 5mol/L NaClO溶液 | D. | 250mL 1mol/L AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑦ | B. | ①②⑥⑧ | C. | ①③④⑧ | D. | ①③⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu丝--电解质;KOH--电解质 | |
| B. | NaCl--电解质;葡萄糖(C6H12O6)--非电解质 | |
| C. | NaCl溶液--非电解质;酒精--非电解质 | |
| D. | O2--不属于电解质或非电解质;MgCl2--非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
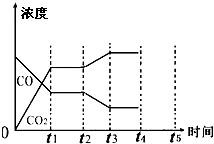 700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中测定的部分数据见表(表中t2>t1):
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中测定的部分数据见表(表中t2>t1):| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.20 | |
| t2 | 0.80 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com