

A.在周期表中,族序数都等于该元素的最外层电子数. |
B.非金属性最强的元素,其氢化物溶于水的酸性最强 |
C.碱金属随原子序数增大,熔点降低;卤族元素的单质,随原子序数增大,熔点依次升高. |
| D.同一周期的主族元素,从左至右,原子半径减小,它们所形成的简单离子半径从左至右依次增大 |
科目:高中化学 来源:不详 题型:填空题
| | IA[ | O族 | ||||||
| 第一周期 | a | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 第二周期 | | | | b | c | d | | |
| 第三周期 | e | | f[ | | | g | h | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 元素性质或原子结构信息 |
| Q | 原子核外有6种不同运动状态的电子 |
| R | 最外层电子数是次外层电子数的3倍 |
| X | 气态氢化物的水溶液呈弱碱性 |
| Y | 第三周期元素的简单离子中离子半径最小 |
| Z | 单质为银白色固体,在空气中燃烧发出黄色火焰 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氦元素位于周期表的第18列 | B.32He和41He互为同位素 |
| C.42He原子核内中子数为2 | D.32He比42He少一个质子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | Al | B | Be | C | Cl | F | Li |
| 电负性 | 1.61 | 2.04 | 1.57 | 2.55 | 3.16 | 3.98 | 0.98 |
| 元素 | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.31 | 3.04 | 0.93 | 3.44 | 2.19 | 2.58 | 1.90 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径(10—10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | — |
| 最低价态 | — | — | -2 | — | -4 | -3 | -1 | — | -3 | -1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
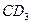 的化合物;C原子比E原子多1个电子;18gC与足量稀硫酸反应,所产生的氢气在标况下的体积为22.4L;C原子中质子数比中子数少1;D原子比A原子多一个质子。则:
的化合物;C原子比E原子多1个电子;18gC与足量稀硫酸反应,所产生的氢气在标况下的体积为22.4L;C原子中质子数比中子数少1;D原子比A原子多一个质子。则:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.s电子绕核旋转,其轨道为一圆圈,而p电子是走∞字形 |
| B.主量子数为1时,有自旋相反的两条轨道 |
| C.主量子数为3时,有3s、3p、3d、3f四条轨道 |
| D.角量子数l决定了原子轨道(电子云)的形状 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com