
| A. | 珍珠、玛瑙、红宝石、水晶的主要成分都是硅酸盐 | |
| B. | 工业上冶炼金属Mg、Cu都采用热还原法 | |
| C. | 氯水、醋酸、小苏打都是电解质 | |
| D. | 利用丁达尔效应可以区别NaCl溶液和Fe(OH)3胶体 |
分析 A、水晶的主要成分是二氧化硅;
B、镁是非常活泼的金属;
C、氯水是混合物;
D、丁达尔效应是胶体所特有的性质.
解答 解:A、珍珠的主要成分为碳酸钙,红宝石的主要成分为氧化铝,水晶的主要成分是二氧化硅,故A错误;
B、镁是非常活泼的金属,需要用电解的方法来冶炼,故B错误;
C、氯水是混合物,既不是电解质也不是非电解质,故C错误;
D、丁达尔效应是胶体所特有的性质,故氢氧化铁胶体有丁达尔效应,而氯化钠溶液无,故D正确.
故选D.
点评 本题考查较为综合,涉及二氧化硅、硅酸盐、金属的冶炼、胶体的性质等知识,为高考常见题型和高频考点,注意把握元素化合物知识的性质和应用,难度不大,学习中注意相关基础知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | Cl2、Br2、I2的沸点逐渐升高,是因为分子间作用力越来越大 | |
| B. | NaOH和NH4Cl化学键类型相同 | |
| C. | N2和CCl4两种分子中,每个原子的最外层都具有8电子稳定结构 | |
| D. | 石英晶体是原子晶体,其分子式为SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
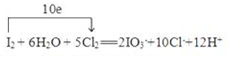 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
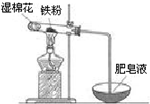 铁是日常生活中用途最广、用量最大的金属材料.
铁是日常生活中用途最广、用量最大的金属材料.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 如果设“此”为电解质,“彼”为非电解质,不是所有的物质都是非此即彼的 | |
| B. | 不是所有反应,都遵循由强(如强酸、强碱、强氧化剂或强还原剂等)制弱(如弱酸、弱碱、弱氧化剂 或弱还原剂等)的规律 | |
| C. | 不是所有自发进行的反应都一定是焓减少的过程 | |
| D. | 在迄今发现的元素中,不一定所有非金属元素(稀有气体除外)都满足条件“主族元素的族序数≥其周期序数” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  操作I导致配制溶液的物质的量浓度偏小 | |
| B. |  用装置II干燥氨气 | |
| C. |  实验Ⅲ可观察铁钉的吸氧腐蚀 | |
| D. |  实验Ⅳ记录的读数为12.20mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com