
| 1 |
| 2 |
| A、H2的燃烧热为-241.8kJ |
| B、2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol |
| C、1molH2完全燃烧生成液态水放出的热量大于241.8kJ |
| D、断开1molH2O的化学键吸收的总能量大于断裂1molH2和0.5 molO2的化学键所吸收的总能量 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、a-c=m-n |
| B、a-b=n-m |
| C、c-d=m+n |
| D、a-c=n+m |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3.2L |
| B、2 L |
| C、1.8 L |
| D、1.5 L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Ca2+)、c(OH-)均增大 |
| B、c(Ca2+)、c(OH-)均保持不变 |
| C、c(Ca2+)、c(OH-)均减小 |
| D、c(OH-)增大、c(H+)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2、SiO2、CO2、CO均为酸性氧化物 |
| B、稀豆浆、硅酸、水玻璃、氯化铁溶液均为胶体 |
| C、烧碱、冰醋酸、四氯化碳、NH3均为电解质 |
| D、BaSO4的水溶液不导电,但BaSO4是强电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
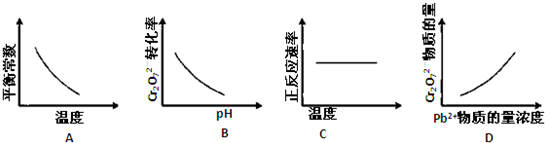
| H+ |
| ①转化 |
| Fe2+ |
| ②还原 |
| OH- |
| ③沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com