
有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、CaCl2、NaCl等物质组成,为鉴定成分,做了如下实验:
(1)将混合物溶于水, 得无色澄清溶液;
得无色澄清溶液;
(2)向此溶液中 滴加BaCl2溶液,有白色
滴加BaCl2溶液,有白色 沉淀产生;
沉淀产生;
(3)过滤后,在白色沉淀中加足量 稀HNO3,沉淀完全溶解。
稀HNO3,沉淀完全溶解。
此推断:混合物中肯定有_____________,肯定没有________,可能有__________。若想进一步确定可能有的物质是否存在,可在(1)溶液中加___________________________溶液的方法来检验。
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:实验题
化学实验是研究化学反应的有效方法。
Ⅰ.ClO2气体是一种高效、广谱、安全的杀菌消毒剂,可用NaClO3和草酸(H2C2O4)反应制得。无水草酸100℃可以升华。某学习小组用下图装置模拟工业制取收集ClO2 。
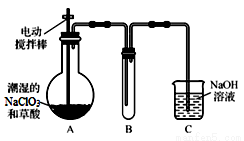
(1) 实验时装置A需在60℃~100℃进行的原因是 ,控制所需温度的方法是 。
实验时装置A需在60℃~100℃进行的原因是 ,控制所需温度的方法是 。
(2)电动搅拌棒的作用是 。装置A中反应产物有Na2CO3、ClO2和CO2等,该反应的化学方程式为 。
(3)在装置C中ClO2和NaOH反应生成等物质的量的两种盐,其中一种盐为NaClO2 ,写出反应的离子方程式 。
Ⅱ. 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
实验编号 | 反应物 | 催化剂 |
① | 10 mL 2% H2O2溶液 | 无 |
② | 10 mL 5% H2O2溶液 | 无 |
③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
(1)实验①和②的目的是_______________________。实验时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是______________________。
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图:

分析上图能够得出的实验结论是________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二12月月考化学试卷(解析版) 题型:选择题
在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀。最终出现黑色沉淀。已知有关物质的溶度积Ksp(25℃)如下,下列叙述错误的是
AgCl | AgI | Ag2S | |
Ksp | 1.8×10-10 | 8.51×10-16 | 6.3×10-50 |
A.沉淀转化的实质就是沉淀溶解平衡的移动
B.溶解度小的沉淀可以转化为溶解度更小的沉淀
C.AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解程度相同
D.25℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海省高二11月月考化学试卷(解析版) 题型:选择题
下列各组热化学方程式中,△H1>△H2的是( )
A.C(s)+O2(g)=CO 2(g) △H1 C(s)+1/2O2(g)=CO(g) △H2
2(g) △H1 C(s)+1/2O2(g)=CO(g) △H2
B.S(g)+O2(g)=SO2(g) △H1 S(s)+O2(g)=SO2(g) △H2
C.2H2(g)+O2(g)= 2H2O(l) △H1 2H2(g)+O2(g)= 2H2O(g) △H2
D.CaCO3(s)=CaO(s)+CO2(g) △H1 CaO(s)+H2O(l)=Ca(OH)2(s) △H2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海省高二11月月考化学试卷(解析版) 题型:选择题
下列说法不符合生产实际的是( )
A.硫酸生产中,SO2催化氧化选择1~10 MPa、400~500 ℃条件下进行
B.尾气中含有少量SO2,可用石灰水吸收,然后再用硫酸处理
C.工业上,通常采用以铁为主的催化剂,在400~500 ℃和10~30 MPa的条件下合成氨
D. 造气中产
造气中产 生的CO,可在催化剂作用下,与水蒸气反应生成CO2和H2
生的CO,可在催化剂作用下,与水蒸气反应生成CO2和H2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高一期中化学卷(解析版) 题型:选择题
甲、乙、丙、丁分别是氢氧化钙溶液、硝酸钾溶液、碳酸钠溶液、盐酸中的一种。已知甲和丙可以反应,甲和丁也可以反应,则下列说法正确的是
 A.甲一定是氢氧化钙溶液 B.乙一定是硝酸钾溶液
A.甲一定是氢氧化钙溶液 B.乙一定是硝酸钾溶液
C.丙不可能是碳酸钠溶液 D.丁只能是盐酸
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高一期中化学卷(解析版) 题型:选择题
某10%NaOH溶液,加热蒸发掉100 g水后得到80mL 20%的溶液,则该20% NaOH溶液的物质的量浓度为
A.6.25 mol/L B.12.5 mol/L C.7 mol/L D.7.5 mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上段考二化学试卷(解析版) 题型:填空题
己知可逆反应AsO43-+2I-+2H+ AsO33-+I2+H2O,设计如下图装置,进行下述操作:
AsO33-+I2+H2O,设计如下图装置,进行下述操作:
①向(Ⅱ)烧杯中逐滴加入浓盐酸,发现微安表(G)指针偏转;②若改往(Ⅱ)烧杯中滴加40%NaOH溶液,发现微安表指针与①的偏转方向相反。回答下列问题
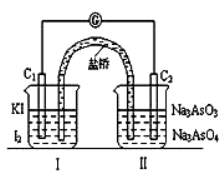
(1)操作①过程中,C1棒为__________极,C2棒上发生的反应为______________________
(2)操作②过程中盐桥中的_________离子移向(I)烧杯,C1棒上发生的反应为_____________
(3)若将微安表换成电解冶炼铝装置,写出电解总反应方程式__________________________________
(4)若将微安表换成电解精炼铜装置,在操作②过程中与C2棒连接的为_________电极,电解一段时间后,溶液中CuSO4溶液的浓度_____________(填“变大”“变小”或“不变”)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省钦州港区高一上11月月考化学卷(解析版) 题型:选择题
在用硫酸铁电化浸出黄铜矿精矿工艺中,有一主要反应:CuFeS2+4Fe3+===Cu2++5Fe2++2S。下列说法正确的是( )
A.反应中硫元素被氧化,所有铁元素均被还原
B.还原剂是S2-和Cu+,氧化剂是Fe3+
C.氧化产物是S,还原产物是Cu2+和Fe2+
D.当转移1 mol e-时,有46 g CuFeS2参加反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com