
����Ŀ���ݱ�����Ħ��������˾������һ���Լ״�Ϊԭ�ϣ���KOHΪ����ʵ������ֻ��Ŀɳ��ĸ�Чȼ�ϵ�أ���һ�ε������ʹ��һ���£���ͼ��һ���绯ѧ���̵�ʾ��ͼ����֪�׳ص��ܷ�ӦʽΪ��2CH3OH+3O2+4KOH![]() 2K2CO3+6H2O����գ�
2K2CO3+6H2O����գ�
��1�����ʱ����ԭ��صĸ������Դ���������������ĵ缫��ӦʽΪ ��
��2���ŵ�ʱ�������ĵ缫��ӦʽΪ ��
��3���ڴ˹���������ȫ��Ӧ���ҳ���A������������648g����׳�������������O2L����״���£���
��4�����ڳ��³�ѹ�£�1gCH3OHȼ������CO2��Һ̬H2Oʱ����22.68kJ����ʾ�÷�Ӧ���Ȼ�ѧ����ʽΪ ��
���𰸡�
��1������4OH����4e��=2H2O+O2��
��2��CH3OH+8OH����6e��=CO32��+6H2O
��3��33.6
��4��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g����H=��1451.52kJ/mol
����������1�����ʱ��ԭ��ظ������Դ��������������������������ʧ���ӷ���������Ӧ���缫��ӦʽΪ��4OH����4e���T2H2O+O2�������Դ�Ϊ������4OH����4e���T2H2O+O2������2���ŵ�ʱ���״�ʧ���Ӻ����������ӷ�Ӧ����̼������Ӻ�ˮ�����Ե缫��ӦʽΪ��CH3OH��6e��+8OH���TCO32��+6H2O��
���Դ�Ϊ��CH3OH��6e��+8OH���TCO32��+6H2O����3���ҳ���B���������ӵõ��ӷ�����ԭ��Ӧ�����ҳ���B������������648g����׳�������������O2���= ![]() =33.6L��
=33.6L��
���Դ�Ϊ��33.6����4��n��CH3OH��= ![]() mol������CO2��Һ̬H2Oʱ����22.68kJ����2molCH3OHȼ�շų�������Ϊ2��22.68kJ��32=1451.52kJ��
mol������CO2��Һ̬H2Oʱ����22.68kJ����2molCH3OHȼ�շų�������Ϊ2��22.68kJ��32=1451.52kJ��
��Ӧ���Ȼ�ѧ����ʽΪ2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g����H=��1451.52kJ/mol��
���Դ�Ϊ��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g����H=��1451.52kJ/mol��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Fe��OH��2���ױ�����������ʵ����������������Һ���ռӦ�Ƶð�ɫ������Fe��OH��2������������ͼ��ʾʵ��װ�ÿ��Ƶô�����Fe��OH��2�������������Ϸֱ�Ϊʯī������ 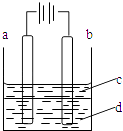
��1��a�缫����Ϊ �� ��缫��ӦʽΪ ��
��2�����Һd������ �� ���ɫ�����ڵ缫�����ɣ�Ҳ������ �� ���ɫ����������֮�����Һ�����ɣ�������ţ�
A����ˮ B��NaCl��Һ C��NaOH��Һ D��CuCl2��Һ
��3��Һ��cΪ������������ �� �ڼ��뱽֮ǰ����d��Һ���м�����д�����Ŀ���� ��
��4��Ϊ���ڶ�ʱ���ڿ�����ɫ�������ɲ�ȡ�Ĵ�ʩ�� �� ������ţ�
A.����ϡ���������Һ
B.�ʵ������Դ��ѹ
C.�ʵ���С���������
D.�ʵ����͵��Һ�¶�
��5����d��ΪNa2SO4��Һ�������һ��ʱ�䣬������ɫ�������ٷ��ӵ�Դ��������⣬���˵缫�Ͽ��������⣬��һ��������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�����ܵõ�Fe2O3 ���ǣ� ��
A.��˿�ڴ�����ȼ��
B.���ȵ�����ˮ������Ӧ
C.��Fe2��SO4��3 ��Һ���ɺ�����
D.����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ�����ڱ��������ǽ���Ԫ�ظ������ҵ�(����)
A. �ư뵼���Ԫ�� B. ��ũҩ��Ԫ��
C. �ƴ�����Ԫ�� D. �����ºϽ��Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���йؽ������ʵ�������ȷ���ǣ� ��
A.�����кܸߵ��۵�
B.�������������� 3 ���Ķ��ǽ���
C.���ܵ��硢����
D.��ֻ�ܺ���ܺͼ����ѧ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ܴ����������( )
A.������H+����Һ�У�CrO42-��Cl-��NO3-��Na+
B.������AlO2-����Һ�У�Na+��K+��NO3-��HCO3-
C.������Al3+����Һ�У�Na+��K+��NO3-��ClO-
D.������CH3COO-����Һ�У�NH4+��Cl-��F-��K+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ�����ڱ������г�112��Ԫ�أ�����Ԫ���������������ǣ� ��
A.��4����
B.��5����
C.��6����
D.��7����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧһ������������ԭ��Ӧ���ǣ�������
A. ���Ϸ�ӦB. �ֽⷴӦC. ���ֽⷴӦD. �û���Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ����һ���Ϊ2 L���ܱ������У�ͨ��112 g N2��24 g��H2 �� ��ʱ������ѹǿΪp����ѹ���ڸ��¶Ⱥʹ��������£�H2��N2��Ӧ�ﵽƽ�⣬���ƽ��ʱѹǿΪ0.95p����ѹ������˵������ȷ����(����)
A.ƽ��ʱ��N2���ʵ�����3.6 mol
B.ƽ��ʱ��H2�����ʵ�����10.8 mol
C.ƽ��ʱ��N2��ת����10%
D.NH3������ٷֺ�����10%
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com