
【题目】如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题.

(1)指出图中明显的错误________________;________________;
(2)A仪器的名称是________________;B仪器的名称是________________;
(3)萃取、分液实验中所用主要玻璃仪器的名称是________________,静置后分液的第一步操作是________________。
 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
【题目】近年来AIST报告正在研制一种“高容量、低成本”的锂—铜空气燃料电池。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O=2Cu+2Li++2OH一,下列说法不正确的是 ( )

A. 放电时,Li+透过固体电解质向Cu极移
B. 放电时,正极的电极反应式为O2+2H2O+4e一=4OH—
C. 通空气时,铜被腐蚀,表面产生Cu2O
D. 通空气时,整个反应过程中,铜相当于是催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿司匹林是一种解毒镇痛药。烃A是一种有机化工原料,下图是以它为初始原料设计合成阿司匹林关系图:
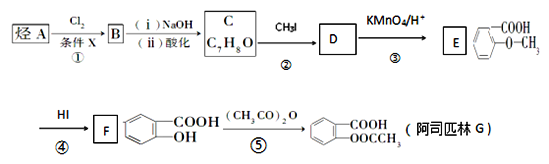
已知:(1)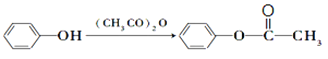
(2)烷基苯在高锰酸钾的作用下,侧链被氧化成羧基:![]()
(3)![]() (苯胺,易被氧化)
(苯胺,易被氧化)
请根据本题所给信息与所学知识回答下列问题:
(1)C的结构简式为__________________________
(2)反应④的反应类型________,在③之前设计②这一步的目的是_____________。
(3)F中含氧官能团的名称__________________________
(4)G(阿司匹林)与足量NaOH溶液反应的化学方程式为_____________________。
(5)符合下列条件的E的同分异构体有________种。写出核磁共振氢谱中有四组峰,峰面积之比为3:2:2:1的结构简式:________________(只写一种)。
a.苯环上有两个取代基
b.遇氯化铁溶液显紫色
c.能发生水解反应
(6)利用甲苯为原料,结合以上合成路线和信息合成功能高分子材料(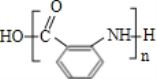 ,无机试剂任选)____________________
,无机试剂任选)____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.1mol/L NaOH溶液400mL。根据溶液的配制情况回答下列问题。
(1)在如图所示仪器中,配制上述溶液肯定不需要的是__________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是__________。

(2)配制时,其正确的操作顺序是(用字母表示,每个操作只用一次)__________。
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1cm~2cm处
(3)关于容量瓶的四种叙述:
①是配制准确浓度溶液的仪器;
②不宜贮存溶液;
③不能用来加热;
④使用之前要检查是否漏水。
这些叙述中正确的是__________(填字母)。
A.①②③④ B.②③ C.①②④ D.②③④
(4)根据计算用托盘天平称取的NaOH固体质量为______。
(5)下面操作造成所配溶液浓度偏高的是__________(填字母)。
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D. 摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,腐蚀严重的青铜器表面大都存在CuCl。关于CuCl在青铜器腐蚀过程中的催化作用,下列叙述可能正确的是
A. 增大了反应的活化能 B. 增大了反应的速率
C. 降低了反应的焓变 D. 增大了反应的焓变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有两组物质的熔点数据如表所示:

根据表中数据回答下列问题。
(1)A组属于________晶体,其熔化时克服的微粒间的作用力是____________。
(2)B组中HF熔点反常是由于__________。
(3)B组晶体不可能具有的性质是________________。
①硬度小 ②水溶液能导电 ③固体能导电 ④液体状态能导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列推断正确的是( )
A. BF3为三角锥形分子
B. NH的电子式为 ,离子呈平面正方形结构
,离子呈平面正方形结构
C. CH4分子中碳的杂化类型与其它有机物中的碳一样,都为sp3杂化
D. CH4分子中的碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成C—H σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用KMnO4和浓盐酸反应制取氯气:KMnO4+HCl(浓)=KCl+MnCl2+Cl2↑+H2O(未配平)。
(1)配平化学方程式,并用单线桥标出电子转移的方向和数目____________。
(2)将上述配平的化学方程式改写为离子方程式________________________。
(3)浓盐酸在反应中显示出来的性质是____________。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若产生0.5 mol Cl2,则被氧化的HCl_______mol,转移的电子的数目约为____。
(5)一定条件下,KMnO4还可以氧化其他还原性物质。__MnO4-+ C2O42-+ = Mn2++ CO2↑+ ,完成上述离子方程式,此反应中,发生氧化反应的物质是______;若转移1 mol电子,生成标准状况下CO2_____L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com