
| A. |  | B. |  | C. |  | D. | 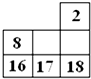 |
分析 根据元素周期表的结构:相邻两个周期同主族元素的原子序数相差2、8、18、32,以此判断同族中位置关系;注意第三列镧系、锕系,长周期第ⅡA族、第ⅢA族之间有10个空列为7个副族和1个Ⅷ族,结合同周期元素根据原子序数判断位置关系,以此来解答.
解答 解:A.1号和11号中间还有3号元素,且1、2元素之间相差17列,故A错误;
B.2号元素为稀有气体He,而7、13为ⅤA族元素,故B错误;
C.10号元素为稀有气体Ne,应该在元素周期表的最右侧,故C错误;
D.8、16为第ⅥA相邻元素,16、17号元素为同周期相邻元素,2、18号元素为0族元素,位置合理,故D正确;
故选D.
点评 本题考查元素周期表的结构及应用,为高频考点,把握元素的位置、原子序数等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:实验题
| 实验用品 | 溶液温度 | 中和热 | |||
| t1 | t2 | △H | |||
| ① | 50mL0.55mol•L-1NaOH | 50mL.0.5mol•L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol•L-1NaOH | 50mL.0.5mol•L-1HCl | 20℃ | 23.5℃ | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
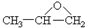
| A. | ①③ | B. | ①⑤ | C. | ②④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相对原子质量逐渐增大 | B. | 原子核外电子排布呈现周期性变化 | ||
| C. | 核电荷数逐渐增大 | D. | 元素的化合价呈现周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体A为SO2和H2的混合物 | B. | 气体A中SO2与H2的体积比为5:1 | ||
| C. | 反应中共消耗Zn 97.5g | D. | 反应中共转移电子3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH2Cl | B. | CH3CHBrCH2Br | C. | CH2BrCH2CH2Br | D. | CH3CHBrCH2CH2Br |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用浓硫酸做干燥剂 | |
| B. | 将火柴梗插入浓硫酸中,火柴梗很快变黑 | |
| C. | 铜与浓硫酸加热时发生反应 | |
| D. | 锌与稀硫酸发生置换反应制取氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com