
(16分)影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol·L-1、2 mol·L-1、18.4 mol·L-1)设计实验方案来研究影响反应速率的因素。甲同学的实验报告如下表:
实验步骤 | 现象 | 结论 |
①分别取等体积的2 mol·L-1的硫酸于试管中 | 反应速率Mg>Fe,Cu不反应 | 金属的性质越活泼,反应速率越快 |
②____________ |
| 反应物浓度越大,反应速率越快 |
(1)甲同学表中实验步骤②为_________________________________________。
(2)甲同学的实验目的是_____________;要得出正确的实验结论,还需控制的实验条件是____________。乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行定量实验。
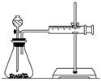
(3)乙同学在实验中应该测定的数据是___________________________________________________。
(4)乙同学完成该实验应选用的实验药品是________,该实验中不选用某浓度的硫酸,理由是___________。
实验二:已知 2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(5)针对上述实验现象,丙同学认为KMnO4与H2C2O4反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是______________的影响。
(6)若用实验证明你的猜想,除高锰酸钾酸性溶液、草酸溶液外,还需要选择的试剂最合理的是________(填字母)。
A.硫酸钾 B.硫酸锰 C.二氯化锰 D.水
(1)向等体积浓度分别为 0.5 mol/L、2 mol/L溶液中投入大小、形状相同的Fe或者Mg
(2)研究金属(或反应物)本身的性质与反应速率的关系 温度相同
(3)测定一定时间内产生气体的体积(或产生一定体积的气体所需时间)
(4)Mg(或Fe)、0.5 mol·L-1硫酸和2 mol·L-1硫酸;常温下Mg和18.4 mol·L-1浓硫酸反应生成SO2;Fe在18.4 mol·L-1浓硫酸中发生钝化;(5)MnSO4(或Mn2+)的催化作用;(6)B;
【解析】
试题分析:(1)甲同学表中实验步骤②为向等体积浓度分别是0.5 mol/L、2 mol/L的硫酸中加入投入大小、形状相同的Fe或者Mg。发现:同一种金属在不同浓度的硫酸中发生反应时,浓度的大的速率快。(2)甲同学的实验目的是研究金属(或反应物)本身的性质与反应速率的关系。要得出正确的实验结论,还需控制的实验条件是反应温度应该相同,这样才能形成对照实验。(3)乙同学在实验中应该测定的数据是相同时间内产生气体的体积的多少或者产生相同体积的气体所需要的时间的长短。若相同的时间内产生的气体体积越大,则反应速率越快;或者收集相同体积的气体,需要的时间越短,则反应速率越快。(4)乙同学完成该实验应选用的实验药品是Mg(或Fe)、0.5 mol·L-1硫酸和2 mol·L-1硫酸;在该实验中不能选用18.4 mol/L硫酸,是因为Fe在浓硫酸中会发生钝化现象;而Mg与18.4 mol/L硫酸发生反应得到硫酸镁、SO2、反应原理发生了改变。(5)针对该实验现象,丙同学认为KMnO4与H2C2O4反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是反应产生的Mn2+对反应起催化剂的作用,使反应速率大大加快。(6)若是Mn2+对反应起催化剂的作用,只要加入的物质中含有+2价的锰元素就可以。分析各个选项,可知应该加入硫酸锰。选项为B。
考点:考查影响化学反应速率的因素的知识。


科目:高中化学 来源:2013-2014天津五区县高一下学期期末考试化学试卷(解析版) 题型:选择题
某同学做完铜、锌稀硫酸原电池的实验后得出了下列结论,你认为正确的是
A.构成原电池正极和负极的材料必须是两种金属
B.当由铜、锌电极与硫酸铜溶液组成原电池时,铜是负极
C.该实验电子沿导线由锌流向铜,氢离子得到电子而放出氢气
D.铜锌原电池工作时,电流由锌经导线流向铜
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省下学期期中考试高二化学试卷(解析版) 题型:填空题
(11分)甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题:
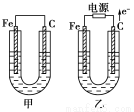
(1)若两池中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的________棒,乙池中的________棒。
②乙池中阳极的电极反应式是_______________________________________________ _。
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式__________________________________________。
②甲池中碳极上电极反应式是____________________,乙池中碳极上电极反应属于____________(填“氧化反应”或“还原反应”)。
③若乙池转移0.02 mol e-后停止实验,该池中溶液体积是200 mL,则溶液混匀后的pH=________。
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省下学期期中考试高二化学试卷(解析版) 题型:选择题
如图是关于反应A2(g)+3B2(g)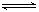 2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是( )
2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是( )
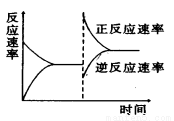
A.升高温度,同时加压 B.降低温度,同时减压
C.增大反应物浓度,同时减小生成物浓度 D.增大反应物浓度,同时使用催化剂
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省下学期期中考试高二化学试卷(解析版) 题型:选择题
某原电池总反应离子方程式为2Fe3++Fe===3Fe2+,能实现该反应的原电池是( )
A.正极为Cu,负极为Fe,电解质溶液为Fe(NO3)2溶液
B.正极为Cu,负极为Fe,电解质溶液为FeCl3溶液
C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3溶液
D.正极为Ag,负极为Fe,电解质溶液为CuSO4溶液
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省下学期期中考试高一化学试卷(解析版) 题型:选择题
下列化学实验事实及其结论都正确的是( )
选项 | 实验事实 | 结论 |
A | 将SO2通入含HClO的溶液中生成H2SO4 | HClO的酸性比H2SO4强 |
B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
C | 稀、浓硝酸分别与铜反应,还原产物分别为NO和NO2 | 稀硝酸氧化性比浓硝酸强 |
D | 将SO2通入溴水中,溴水褪色 | SO2具有漂白性 |
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省下学期期中考试高一化学试卷(解析版) 题型:选择题
下列说法中正确的是 ( )
A.6.8 g固体KHSO4与3.9 g固体Na2O2中阴离子数目相同
B.常温下铁、铜均不溶于浓硫酸, 说明常温下铁、铜与浓硫酸均不反应
C.离子化合物中只含离子键
D.中子数为18的氯原子可表示为18Cl
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省资阳市高一下学期期末考试化学试卷(解析版) 题型:简答题
(5分)某含C、H、O三种元素的有机物4.6 g完全燃烧,若将生成的气体全部通过浓硫酸,则浓硫酸质量增加5.4 g;若将生成的气体全部通过足量的过氧化钠,过氧化钠的质量增加6.2 g(假定气体全部吸收)。
(1)试通过计算推断该有机物的分子式。
(2)该有机物有多种同分异构体,其中一种能和Na反应生成H2,请试写出该有机物的结构简式:________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省资阳市二下学期期末考试化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式是
A.NaHCO3的水【解析】
HCO3-+H2O=CO32-+H3O+
B.用银氨溶液检验乙醛的醛基:
CH3CHO+2Ag(NH3)2OH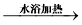 CH3COO-+NH4++3NH3+2Ag↓+H2O
CH3COO-+NH4++3NH3+2Ag↓+H2O
C.向苯酚钠溶液中通入少量的CO2:CO2+H2O+2C6H5O-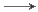 2C6H5OH+2CO32-
2C6H5OH+2CO32-
D.泡沫灭火剂的原理:Al3++3HCO3-=Al(OH)3↓+3CO2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com