
 (2)Cl-
(2)Cl-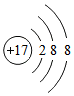 .
. 科目:高中化学 来源: 题型:选择题
| 化学键 | N≡N | F-F | N-F |
| 键能:kJ/mol | 941.7 | 154.8 | 283.0 |
| A. | 过程F2(g)→2F(g)吸收能量 | |
| B. | 过程N(g)+3F(g)→NF3(g) 放出能量 | |
| C. | 反应N2(g)+3F2(g)=2NF3(g) 放出能量 | |
| D. | NF3吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
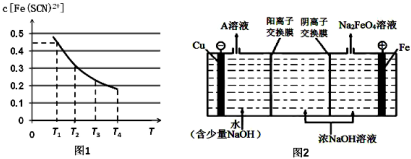
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 浓硫酸(H2SO4)500mL | |
| 浓度(质量分数) | 98% |
| 密度 | 1.81g•cm-3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封贮藏 | |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
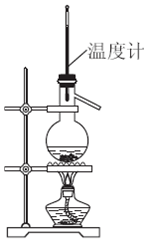
| A. | 制取乙烯 | |
| B. | 制取氯气 | |
| C. | 分离乙醇和水 | |
| D. | 分离水和碘的四氯化碳(常压下沸点76.8℃)溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
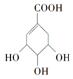 ,关于它的叙述中不正确的是( )
,关于它的叙述中不正确的是( )| A. | 该有机物能使溴的四氯化碳溶液褪色 | |
| B. | 该有机物发生消去反应可得到芳香烃 | |
| C. | 该有机物在一定条件下可发生氧化反应 | |
| D. | 1 mol该有机物最多可与1 mol NaHCO3反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com