
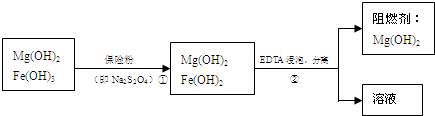
(1)除去Mg粉中的Al粉的离子方程式为 ;
(2)除去FeCl2溶液中少量CuCl2杂质的试剂是 ,离子方程式为 ;
(3)加热条件下铁与水蒸气反应的化学反应方程式为 ;
(4)Fe(OH)2露置于空气中转化Fe(OH)3的化学反应方程式为 ;
(1)2Al+2OH-+2H2O=2AlO2-+3H2↑(2分)
(2)铁 (1分) Fe+ Cu 2+=Fe2+ Cu(2分)
(3)3Fe+4H2O(g) Fe3O4+4H2(2分)
Fe3O4+4H2(2分)
(4)4Fe(OH)2+O2+2H2O=4Fe(OH)3(2分)
【解析】
试题分析:(1)铝能溶于氢氧化钠溶液中,所以要除去Mg粉中的Al粉可以用氢氧化钠溶液,反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑。
(2)铁能和氯化铜反应生成铜和氯化亚铁,所以除去FeCl2溶液中少量CuCl2杂质,所需要的试剂是铁粉,反应的离子方程式是Fe+ Cu 2+=Fe2+ Cu。
(3)在加热的条件下,铁能和水蒸气反应生成四氧化三铁和氢气,反应的化学方程式是3Fe+4H2O(g) Fe3O4+4H2。
Fe3O4+4H2。
(4)氢氧化亚铁极易被氧化生成氢氧化铁,所以Fe(OH)2露置于空气中转化Fe(OH)3的化学反应方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3。
考点:考查物质的除杂、铁及其化合物的性质
点评:该题是基础性试题的考查,难度不大。该题主要是考查学生对基础知识的了解掌握情况,有利于培养学生的应试能力,提高学生的学习效率。该题的关键是熟练记住有关物质的化学性质,并能灵活运用即可。


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:阅读理解
| 1 |
| 2 |
| 1 |
| 2 |
| 精制阻燃剂的条件 | 阻燃剂铁含量 | |||
| 序号 | 提纯体系温度T/℃ | 加入EDTA质量(g) | 加入保险粉质量(g) | W(Fe)/(10-4g) |
| 1 | 40 | 0.05 | 0.05 | 7.63 |
| 2 | 40 | 0.05 | 0.10 | 6.83 |
| 3 | 60 | 0.05 | 0.10 | 6.83 |
| 4 | 60 | 0.10 | 0.10 | 6.51 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 (2012?百色二模)某化学兴趣小组的同学想验证Mg与CO2的反应.可以选用的药品:浓硫酸、稀盐酸、稀硫酸、镁粉、大理石、澄清石灰水、饱和NaHCO3溶液、饱和Na2CO3溶液可以选用的装置:如右图所示(必要时装置可重复使用,彼此连接成一套完整的实验装置)
(2012?百色二模)某化学兴趣小组的同学想验证Mg与CO2的反应.可以选用的药品:浓硫酸、稀盐酸、稀硫酸、镁粉、大理石、澄清石灰水、饱和NaHCO3溶液、饱和Na2CO3溶液可以选用的装置:如右图所示(必要时装置可重复使用,彼此连接成一套完整的实验装置)| 选用的装置 | 加入的剂 | 作用 |
A A |
稀盐酸、大理石 稀盐酸、大理石 |
产生CO2气体 产生CO2气体 |
B B |
饱和的NaHCO3溶液 饱和的NaHCO3溶液 |
除去二氧化碳中的氯化氢杂质 除去二氧化碳中的氯化氢杂质 |
B B |
浓H2SO4 浓H2SO4 |
干燥二氧化碳气体 干燥二氧化碳气体 |
C C |
镁粉 镁粉 |
镁和二氧化碳反应 镁和二氧化碳反应 |
| B | 澄清石灰水 | 吸收多余CO2 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2012-2013年黑龙江哈尔滨第十二中学高一上学期期末考试化学试卷(带解析) 题型:填空题
(1)除去Mg粉中的Al粉的离子方程式为 ;
(2)除去FeCl2溶液中少量CuCl2杂质的试剂是 ,离子方程式为 ;
(3)加热条件下铁与水蒸气反应的化学反应方程式为 ;
(4)Fe(OH)2露置于空气中转化Fe(OH)3的化学反应方程式为 ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com