
【题目】N2+3H2 ![]() 2NH3,是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
2NH3,是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
A. 降低体系温度能加快反应速率
B. 使用恰当的催化剂能加快反应速率,又能提高N2的转化率
C. 达到反应限度时各组分含量之比一定等于3∶1∶2
D. 若在反应的密闭容器加入1mol N2和过量的H2,最后不能生成2mol NH3
科目:高中化学 来源: 题型:
【题目】利用废镀锌铁皮制备磁性Fe3O4胶体粒子及副产物ZnSO4晶体的实验流程如下:

已知:Zn及其化合物的性质与Al及其化合物的性质相似。
(1)用NaOH溶液处理废镀锌铁皮除溶解锌外,另一个作用是_______________。为缩短用NaOH溶液处理废镀锌铁皮的时间,可采取的措施是_____________(答两条)。
(2)加入适量H2O2溶液的主要作用是______________。溶液B中n(Fe2+):n(Fe3+)=______。
(3)在由溶液B制得Fe3O4胶体粒子的过程中,须缓慢滴加稀NaOH溶液并持续通入N2,持续通入N2的原因是_____________________。
(4)请补充完整下列由溶液A获得副产品ZnSO4晶体的实验步骤:
①向溶液A中通入CO2气体,得到Zn (OH)2沉淀;
②______________、洗涤得到沉淀;
③______________;
④将溶液加热浓缩、冷却结晶、过滤、洗涤、干燥即可得到产品。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海藻中含有丰富的、以离子形式存在的碘元素。下图是实验室从海藻里提取碘的流程中的一部分。

下列判断正确的是
A. 步骤①③的操作分别是过滤、萃取
B. 可用淀粉溶液检验步骤②的反应是否进行完全
C. 步骤③中加入的有机溶剂是裂化汽油或乙醇
D. 步骤④的操作是过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国是世界上最早制得和使用金属锌的国家。一种以闪锌矿(主要成份是ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:

相关金属离子[c(Mn+)=0.10mol·L–1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
开始沉淀的pH | 1.5 | 6.3 | 6.3 | 7.4 |
沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 |
回答下列问题:
(1)写出ZnS的电子式__________________________;
焙烧过程中主要反应的化学方程式为__________________________。
(2)滤渣1的成分为:___________________;
(3)试剂Y是_________(只要求填写一种), 调PH值的范围是___________________。
(4)电解硫酸锌溶液制备单质锌时,电解的总反应离子方程式为:___________________。
(5)为将溶液中的Fe2+氧化,试剂X可选用的是_______。(填序号)
A.H2O2 B.H2S C.HNO3 D.O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔、乙烯均是重要的化工原料。回答下列问题:
(1)1902年,Sabatier首次发现,常压下过渡金属可以催化含有双键或叁键的气态烃的加氢反应。
①已知:C2H2(g)+H2(g)═C2H4(g)△H1=-174.3kJ·mol—1
K1(300K)=3.37×1024
C2H2(g)+2H2(g)=C2H6(g)△H2═-311.0kJ·mol一l
K2(300K)═1.19×1042
则反应C2H4(g)+H2(g)═C2H6(g)的△H=___kJ·mol一1,K(300K)=__(保留三位有效数字)。
②2010年Sheth等得出乙炔在Pd表面选择加氢的反应机理(如图)。其中吸附在Pd表面上的物种用*标注。
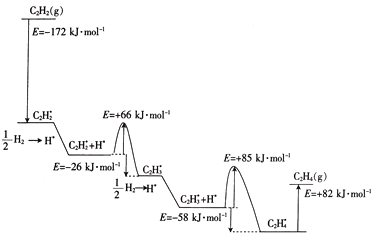
上述吸附反应为____(填“放热”或“吸热”)反应,该历程中最大能垒(活化能)为____kJ·mol-1,该步骤的化学方程式为____。
(2)在恒容密闭容器中充入乙烯,一定条件下发生反应C2H4(g)C2H2(g)+H2(g)。乙烯的离解率为a,平衡时容器内气体总压强为P总,则分压p(C2H4)═___(用p总和a表示)。
(3)用如图装置电解含CO2的某酸性废水溶液,阴极产物中含有乙烯。
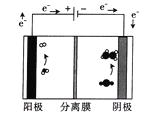
该分离膜为___(填“阳”或“阴”)离子选择性交换膜;生成乙烯的电极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4-CO2催化重整不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。
已知:CH4(g)+O2(g)=CO2(g)+2H2(g)ΔH=-319kJ·mol1
CO(g)+1/2O2(g)=CO2(g)ΔH=-283kJ·mol1
回答下列问题:
(1)写出CH4-CO2催化重整反应的热化学方程式:_______________________________。
(2)某温度下,向密闭容器中充入CH4与CO2,发生CH4-CO2催化重整反应。测得平衡混合物中CO(g)的体积分数[φ(CO)]与起始投料比Z[Z=n(CH4)/n(CO2)]的关系如图所示;

①当Z=2时,CO2的平衡转化率ɑ=__________%。
②当Z=3时,反应达到平衡状态后,CO的体积分数可能是图1中的_________点(填“C”、“D”或“E”)。
(3)若CO2的平衡转化率(a)与温度(T)、压强(p)的关系如图所示。

①由图可知压强p1__________p2(选填“>”、“<“或“=”);
②在温度为T5℃,压强为P1条件下,向2L密闭容器中充入1molCH4与1molCO2发生CH4-CO2催化重整反应,则此条件下该反应的平衡常数为:_____________________;达平衡后若再充入1.5molCH4、1.5molCO2、1molCO、1molH2,则此时v正_______v逆(选填“>”、“<“或“=”);在该条件下,以下能说明该反应已达平衡的是________________。
A.CH4与CO2的物质的量比为1:1
B.氢气的体积分数不变
C.混合气体的平均摩尔质量保持不变
D.当消耗1mol的CO2同时,有2mol的CO生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用如图所示装置进行化学反应X+2Y=2Z能量变化情况的研究。当向试管中滴加试剂Y时,观察到U形管中液面甲处下降、乙处上升。下列关于该反应的叙述正确的是( )
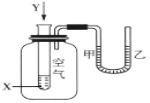
①该反应为放热反应
②该反应为吸热反应
③生成物的总能量比反应物的总能量高
④反应物的总能量比生成物的总能量高
⑤该反应过程可以看成贮存于X、Y内部的部分能量转化为热能而释放出来
A.仅①④⑤B.仅①④C.仅①③D.仅②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有显著抗癌活性的10-羟基喜树碱的结构如图所示,

下列关于10-羟基喜树碱的说法正确的是
A. 10-羟基喜树碱属于芳香烃
B. 分子式为:C20H16N2O5
C. 不能发生酯化反应
D. 一定条件下,1mol该物质可与9molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(7分)某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A![]() H++HA- HA-
H++HA- HA-![]() H++A2-
H++A2-
试完成下列问题:
(1)Na2A溶液显 (填“酸性”“中性”或“碱性”)。理由是
(用离子方程式表示)。
(2)在0.1 mol·L-1的Na2A溶液中,下列粒子浓度关系式正确的是 。A.c(A2-)+c(HA-)+c(H2A)=0.1 mol·L-1
B.c(OH-)=c(H+)+c(HA-)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-)
D.c(Na+)=2c(A2-)+2c(HA-)
(3)已知0.1 mol·L-1 NaHA溶液的pH=2,则0.1 mol·L-1H2A溶液中氢离子的物质的量浓度可能是 0.11 mol·L-1(填“<”、“>”或“=”),理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com