
分析 (1)①2Zn(s)+O2(g)═2ZnO(s)△H1
②Hg(l)+1/2O2(g)═HgO(s)△H2
①×$\frac{1}{2}$-②得:Zn(s)+HgO(s)═ZnO(s)+Hg(l),依据盖斯定律计算反应热;
(2)①N2(g)+3H2(g)=2NH3(g)△H1
②2H2(g)+O2(g)=2H2O(l)△H2
③4NH3(g)+O2(g)=2N2H4(l)+2H2O(I)△H3
则:-③×$\frac{1}{2}$--①+$\frac{3}{2}$×②得:N2H4(l)+O2(g)═N2(g)+2H2O(l),依据盖斯定律计算反应热,书写热化学方程式.
解答 解:(1)①2Zn(s)+O2(g)═2ZnO(s)△H1
②Hg(l)+1/2O2(g)═HgO(s)△H2
①×$\frac{1}{2}$-②得:Zn(s)+HgO(s)═ZnO(s)+Hg(l)△H,依据盖斯定律可知:△H=$\frac{1}{2}$×△H1-△H2;
故答案为:$\frac{1}{2}$×△H1-△H2;
(2)①N2(g)+3H2(g)=2NH3(g)△H1
②2H2(g)+O2(g)=2H2O(l)△H2
③4NH3(g)+O2(g)=2N2H4(l)+2H2O(I)△H3
则:-③×$\frac{1}{2}$--①+$\frac{3}{2}$×②得:N2H4(l)+O2(g)═N2(g)+2H2O(l),△H,依据盖斯定律得△H=-$\frac{1}{2}$△H3-△H1+$\frac{3}{2}$△H2,所以该反应的热化学方程式:N2H4(l)+O2(g)═N2(g)+2H2O(l),△H=-$\frac{1}{2}$△H3-△H1+$\frac{3}{2}$△H2,
故答案为:N2H4(l)+O2(g)═N2(g)+2H2O(l),△H=-$\frac{1}{2}$△H3-△H1+$\frac{3}{2}$△H2,
点评 本题考查了反应热的计算,侧重考查利用盖斯定律计算反应热,解题关键如何利用已知方程式运算得到目标方程式是解题关键,题目难度中等.


科目:高中化学 来源: 题型:推断题
| 单质 | A | B | C | D | E |
| 最高价氧化物 对应水化物的稳定性 | 难分解 | 能分解 | 能分解 | 能分解 | 能分解 |
| 单质性质 | 与水剧烈反应 | 缓慢溶于热水 | 溶于强碱性溶液 | 难溶于冷的浓硝酸 | 溶于浓、稀硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 化学键 | C-H | C-C | C═C | H-H |
| 键能/kJ•mol-1 | 412 | 348 | 612 | 436 |
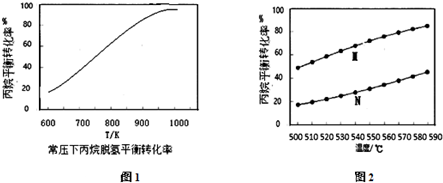
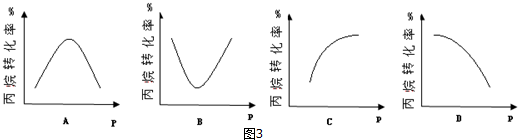
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
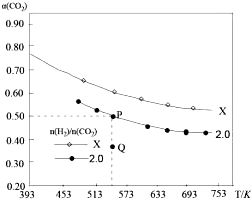 在两个固定容积均为1L密闭容器中以不同的氢碳比$\frac{n({H}_{2})}{n(C{O}_{2})}$充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2 (g)?C2H4(g)+4H2O(g)△H.CO2的平衡转化率a(CO2)与温度的关系如图所示.下列说法正确的是( )
在两个固定容积均为1L密闭容器中以不同的氢碳比$\frac{n({H}_{2})}{n(C{O}_{2})}$充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2 (g)?C2H4(g)+4H2O(g)△H.CO2的平衡转化率a(CO2)与温度的关系如图所示.下列说法正确的是( )| A. | 该反应在高温下自发进行 | |
| B. | X的氢碳比X>2.0,且Q点在氢碳比为2.0时v(正)<v(逆) | |
| C. | 若起始时,CO2、H2浓度分别为0.5mol/L和1.0mol/L,则可得到P点,对应温度的平衡常数的值为512 | |
| D. | 向处于P点状态的容器中,按2:4:1:4的比例再充入CO2、H2、C2H4、H2O,再次平衡后a(CO2)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
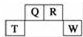 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
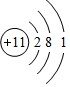 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com