
【题目】![]() 为阿伏加德罗常数的值。下列说法正确的是( )
为阿伏加德罗常数的值。下列说法正确的是( )
A. 5.6![]()
![]() 在氧气中燃烧,完全反应时转移电子数为0.3
在氧气中燃烧,完全反应时转移电子数为0.3![]()
B. 标准状况下,4.48![]()
![]() 中所含原子数为
中所含原子数为![]()
C. 1![]()
![]() 的
的![]() 溶液中含有的
溶液中含有的![]() 数为0.2
数为0.2![]()
D. 常温下,1.7![]()
![]() 和3.65
和3.65![]()
![]() 混合后,气体分子数为0.2
混合后,气体分子数为0.2![]()
科目:高中化学 来源: 题型:
【题目】化合物I(C11H12O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基。I可以用E和H在一定条件下合成:

已知以下信息:
①A的核磁共振氢谱表明其只有一种化学环境的氢;
②R--CH==CH2![]() R—CH2CH2OH;
R—CH2CH2OH;
③化合物F苯环上的一氯代物只有两种;
④通常在同一个碳原子上连两个羟基不稳定,易脱水形成羰基。
回答下列问题:
(1)A的化学名称为___________________。B分子中最多共面原子数为_________。
(2)F的结构简式为___________________。
(3) A生成B的化学方程式为________________________________该反应类型为___________。
(4)E、H生成I的化学方程式为____________________________________________。
(5)已知:J比I(C11H12O3)相对分子质量小14,J的同分异构体中能同时满足如下条件的共有__________种。
①苯环上只有两个取代基,
②既能发生银镜反应,又能与饱和NaHCO3溶液反应放出CO2。
(6)J的一个同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2∶2∶1,写出J的这种同分异构体的结构简式_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】改变0.1![]() 二元弱酸
二元弱酸![]() 溶液的pH,溶液中的
溶液的pH,溶液中的![]() 、
、![]() 、
、![]() 的物质的量分数
的物质的量分数![]() 随pH的变化如图所示[已知
随pH的变化如图所示[已知![]() ]。
]。

下列叙述错误的是
A.pH=1.2时,![]()
B.![]()
C.Ph=2.7时,![]()
D.pH=4.2时,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质](15分)
我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。回答下列问题:
(1)氮原子价层电子对的轨道表达式(电子排布图)为_____________。
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图(a)所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是___________;氮元素的E1呈现异常的原因是__________。
(3)经X射线衍射测得化合物R的晶体结构,其局部结构如图(b)所示。
①从结构角度分析,R中两种阳离子的相同之处为_________,不同之处为__________。(填标号)
A.中心原子的杂化轨道类型 B.中心原子的价层电子对数
C.立体结构 D.共价键类型
②R中阴离子N5-中的σ键总数为________个。分子中的大π键可用符号![]() 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为![]() ),则N5-中的大π键应表示为____________。
),则N5-中的大π键应表示为____________。
③图(b)中虚线代表氢键,其表示式为(NH4+)N-H┄Cl、____________、____________。

(4)R的晶体密度为d g·cm-3,其立方晶胞参数为a nm,晶胞中含有y个[(N5)6(H3O)3(NH4)4Cl]单元,该单元的相对质量为M,则y的计算表达式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2017天津]常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A.增加c(CO),平衡向正向移动,反应的平衡常数增大
B.第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
C.第二阶段,Ni(CO)4分解率较低
D.该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
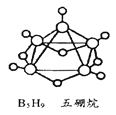
【题目】(1)2008年北京奥运会主体育场的外形好似“鸟巢”(The Bird Nest),有一类化学物质也好似鸟巢,如化学式是B5H9的五硼烷(如图)。 请问五硼烷的摩尔质量是____g/mol。

(2)在同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为______,质量之比为______,密度之比为________。
现有三组混合物:①溴水 ②39%的乙醇溶液(乙醇的沸点为78.4℃)③汽油和氯化钠溶液,分离以上各混合物的正确实验方法依次是_______ 、________、_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂的化合物用途广泛,如Li3N是非常有前途的储氢材料,氨基锂(LiNH2)主要用于药物制造。在一定条件下,2.30 g固体A与5.35 g NH4Cl固体恰好完全反应,生成固体B和4.48 L气体C(标准状况),气体C极易溶于水得到碱性溶液,电解无水B可生成一种短周期元素的金属单质D和氯气。由文献资料知道:工业上物质A可用金属D与液态的C在硝酸铁催化下反应来制备,纯净的A为白色固体,但制得的粗品往往是灰色的;A的熔点390℃,沸点430℃,密度大于苯或甲苯,遇水反应剧烈,也要避免接触酸、酒精。在空气中A缓慢分解,对其加强热则猛烈分解,在750~800℃分解为Li3N和气体C。
回答下列问题:
(1)C的电子式为 。
(2)将锂在纯氮气中燃烧可制得Li3N,其反应的化学方程式为 。
(3)氮化锂在氢气中加热时可得到氨基锂(LiNH2),其反应的化学方程式为:Li3N+2H2![]() LiNH2+2LiH,氧化产物为 (填化学式)。在270℃时,该反应可逆向发生放出H2,因而氮化锂可作为储氢材料,储存氢气最多可达Li3N质量的 (精确到0.1)。
LiNH2+2LiH,氧化产物为 (填化学式)。在270℃时,该反应可逆向发生放出H2,因而氮化锂可作为储氢材料,储存氢气最多可达Li3N质量的 (精确到0.1)。
(4)A在750~800℃分解的方程式 。
(5)亚氨基锂(Li2NH)也是一种储氢容量高,安全性好的固体储氢材料,其储氢原理可表示为Li2NH+H2![]() LiNH2+LiH,下列有关说法正确的是 。
LiNH2+LiH,下列有关说法正确的是 。
A.Li2NH中N的化合价是1 B.该反应中H2既是氧化剂又是还原剂
C.Li+和H的离子半径相等 D.此法储氢和钢瓶储氢的原理相同
(6)久置的A可能大部分变质而不能使用,需要将其销毁。遇到这种情况,可用苯或甲苯将其覆盖,然后缓慢加入用苯或甲苯稀释过的无水乙醇,试解释其化学原理 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
A.0.1 mol 的![]() 中,含有
中,含有![]() 个中子
个中子
B.pH=1的H3PO4溶液中,含有![]() 个
个![]()
C.2.24L(标准状况)苯在O2中完全燃烧,得到![]() 个CO2分子
个CO2分子
D.密闭容器中1 mol PCl3与1 mol Cl2反应制备 PCl5(g),增加![]() 个P-Cl键
个P-Cl键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,干燥圆底烧瓶中充满NO2和O2的混合气体进行喷泉实验,经充分反应后,瓶内充满水,则瓶内水溶液的物质的量浓度为
A. 5/112 B. 1/28 C. 2/49 D. 8/245
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com