
| A. | 纳米碳管是一种新型的高分子化合物 | |
| B. | 纳米碳管的化学性质稳定 | |
| C. | 纳米碳管的结构和性质与金刚石相同 | |
| D. | 纳米碳管导电属于化学变化 |
分析 A.纳米碳管只含一种元素;
B.碳单质在常温下的化学性质稳定;
C.碳纳米管是管状结构,金刚石是立体网状结构;
D.纳米碳管导电的过程中没有新物质生成.
解答 解:A.碳纳米管是由碳原子组成的单质,只有一种元素,不属于化合物,故A错误;
B.碳单质在常温下的化学性质稳定,所以纳米碳管的化学性质稳定,故B正确;
C.碳纳米管是管状结构,金刚石是立体网状结构,两者结构不同;由于碳原子的排列方式不同,性质也不完全相同,故C错误;
D.纳米碳管导电的过程中没有新物质生成,属于物理变化,故D错误;
故选B.
点评 本题主要考查纳米材料,考查学生获取信息,筛选信息结合已有知识分析、解决问题的能力,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
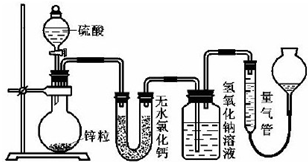
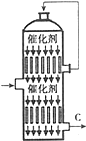 硫酸的年产量高低常用于衡量一个国家化工生产水平的高低.
硫酸的年产量高低常用于衡量一个国家化工生产水平的高低.| 压强 (Pa) 温度 (℃) | 1.013×105 | 5.065×105 | 10.13×105 | 15.195×105 |
| 400 | 99.61% | 99.72% | 99.84% | 99.88×105 |
| 500 | 96.75% | 97.67% | 98.52% | 98.94% |
| 600 | 85.20% | 88.97% | 92.76% | 94.68% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 组成元素相同且各元素质量分数也相同的一定互为同分异构体 | |
| B. | 相对分子质量相同的有机物一定为同分异构体 | |
| C. | 有相同的分子通式且分子组成上相差一个或若干个CH2原子团的物质一定互为同系物 | |
| D. | 结构不同,性质相似,化学式相同的物质互称同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,该化合物中含有的化学键有离子键、共价键
,该化合物中含有的化学键有离子键、共价键查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 加入催化剂,该化学反应的活化能和反应热都改变 | |
| B. | b曲线是加入催化剂时的能量变化曲线 | |
| C. | 该反应的热化学方程式为N2(g)+3H2(g)?2NH3(g);△H=-92kJ•mol-1 | |
| D. | 在温度、体积一定的条件下,通入lmol N2和3molH2 反应后放出的热量为Q1kJ,则Q1<92 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=4的盐酸中:c(H+)=4.0mol•L-1 | |
| B. | NH4Cl溶液中:c(Cl-)=c(NH4+) | |
| C. | NaCl溶液中:c(Na+)+c(H+)=c(Cl-)+c(OH-) | |
| D. | Na2CO3溶液中:c(HCO3-)+c(H2CO3)+c(CO32-)=2c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇能使酸性KMn04溶液和酸性K2Cr207溶液褪色,均被氧化成乙酸 | |
| B. | 向酸性高锰酸钾中加入草酸溶液,随着反应的进行,反应速率逐渐减小 | |
| C. | 向某溶液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该溶液中存在S042-或S032- | |
| D. | 实验室提纯混有少量氯化钠的硝酸钾,通常采用重结晶的方法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com