
【题目】某研究性学习小组对某废旧合金(含有Cu、Fe、Si 三种成分)进行分离、回收。其工业流程如图:
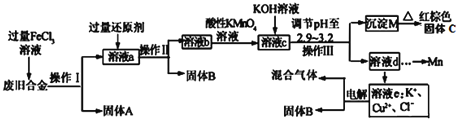
已知:298K时,Ksp[Cu(OH)2]=2.0×10-20,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=1.9×10-13,根据上面流程回答有关问题:
(1)操作Ⅰ、Ⅱ、Ⅲ一定都不含有的操作是________
A.过滤 B.洗涤 C.干燥 D.蒸馏
(2)过量的还原剂应是________,溶液a中发生的反应的离子方程式为________;
(3)将溶液c调节pH至2.9~3.2的目的是________;
(4)常温下,取2mol/L的CuCl2溶液,若要使Cu2+开始沉淀,应调节pH至________;
(5)工业上由红棕色固体C制取相应单质常用的方法是________。
A.电解法 B.热还原法 C.热分解法
(6)用惰性电极电解溶液e制取固体B,阳极主要发生的电极反应为______________。
【答案】D Cu ![]() 使Fe3+完全沉淀,同时避免Cu2+等其他金属阳离子沉淀 4 B
使Fe3+完全沉淀,同时避免Cu2+等其他金属阳离子沉淀 4 B ![]()
【解析】
废旧合金中含有Fe,Cu和Si三种成分,最终要实现分离和回收;第一步向废旧合金中加过量的FeCl3,Si无法反应,Fe和Cu则会被溶解;因此固体A即未反应的Si,溶液a中则含有Fe2+,Cu2+以及未消耗完的Fe3+;那么第二步中加还原剂则是为了去除Fe3+,为了不引入新的杂质,可能的选择为Fe粉或Cu粉;又因为,溶液e中含有Cu2+,而加入过量的Fe粉会使Cu2+被还原为单质,因此还原剂应选择铜粉;因此固体B即未反应完的铜粉,溶液b中则含有Fe2+,Cu2+;溶液b中加酸性高锰酸钾溶液,可以将Fe2+转变为Fe3+,调节pH值时就可将Fe3+从溶液中沉淀除去,同时又可避免Cu2+在这一步中沉淀;脱除溶液d中的Mn元素后,溶液e中的所有离子仅剩Cu2+,K+和Cl-,再对其进行电解处理即可得到铜单质以及其他产物。
(1)操作Ⅰ,Ⅱ,Ⅲ都是分离溶液和固体的操作,除过滤外还会涉及洗涤和干燥的步骤;蒸馏是用来分离液体互溶的体系,因此上述操作中一定不涉及蒸馏;
(2)通过分析可知,还原剂应当选择铜粉,利用铜粉将第一步中剩余的Fe3+除去;相关的离子方程式为:![]() ;
;
(3)由题可知,常温下![]() ,
,![]() ,
,![]() ,因此同等浓度下溶液中Fe3+先发生沉淀,后续是Cu2+,最后时候Mn2+,因此调节pH值在2.9至3.2,目的是使Fe3+沉淀完全的同时避免Cu2+等其他金属离子发生沉淀;
,因此同等浓度下溶液中Fe3+先发生沉淀,后续是Cu2+,最后时候Mn2+,因此调节pH值在2.9至3.2,目的是使Fe3+沉淀完全的同时避免Cu2+等其他金属离子发生沉淀;
(4)由题可知,常温下![]() ,铜离子浓度为2mol/L时,若要开始生成Cu(OH)2沉淀,OH-的浓度至少为10-10mol/L,即pH至少为4;
,铜离子浓度为2mol/L时,若要开始生成Cu(OH)2沉淀,OH-的浓度至少为10-10mol/L,即pH至少为4;
(5)通过分析可知,红棕色固体C即为Fe2O3,由其获取Fe单质,采用的是热还原法;
(6)溶液中含有Cl-,因此惰性电极电解该溶液时,阳极发生的是Cl-的氧化反应,电极反应为:![]() 。
。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】下列说法或表达正确的是( )
①活性炭、SO2和HClO都具有漂白作用,且漂白原理相同
②向100mL0.1mol/L 的溴化亚铁溶液中通入0.05mol的氯气时发生反应的离子方程式:2Fe2++4Br-+3Cl2=2 Fe3++2Br2+6Cl-
③电解精炼铜时,以粗铜作阴极,纯铜作阳极
④钢铁的吸氧腐蚀负极电极反应式 :Fe-3e-=Fe3+
⑤碳酸氢根离子的电离方程式可表示为: HCO3- + H2O![]() H3O++ CO32-
H3O++ CO32-
⑥SiO2 虽是酸性氧化物,但其不溶于水,因此不能与NaOH溶液反应
⑦ CO、SO2、NO、NO2都是对大气产生污染的气体,他们在空气中都能稳定存在
⑧浓硫酸具有脱水性,所以可以做干燥剂
A.②④⑧ B.②⑤ C.③④⑥ D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼化钒(VB2)空气电池是目前储电能力最高的电池,电池示意图如图,该电池工作时发生的反应为:4VB2+11O2=4B2O3+2V2O5。下列说法不正确的是( )
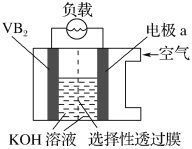
A.电极a为电池正极
B.电池工作过程中,电极a附近区域pH减小
C.图中选择性透过膜为阴离子透过膜
D.VB2极发生的电极反应为:2VB2+22OH--22e-=V2O5+2B2O3+11H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是“国际化学元素周期表年”。1869年门捷列夫把当时已知的元素根据物理、化学性质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下所示。下列说法错误的是

A.甲位于现行元素周期表第四周期第ⅢA族
B.原子半径比较:甲>乙>Si
C.原子序数:甲-Ca=1
D.推测乙的单质可以用作半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】6.4g铜投入一定浓度的HNO3中,铜完全溶解,生成NO和NO2的混合气体,用试管全部收集,得到标准状况下的体积为2240mL。请回答:
(1)反应中消耗掉HNO3的物质的量为___mol。
(2)生成NO2的体积(标况)为___mL。
(3)将盛有混合气体的试管倒扣在水槽中,通入标况下的O2,恰好使气体完全溶于水中,则通入O2的体积是___mL。(请写出解答过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中各组物质之间不能通过一步反应实现如图的是( )
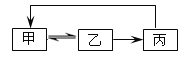
甲 | 乙 | 丙 | |
A | NaHCO3 | Na2CO3 | NaCl |
B | SiO2 | H2SiO3 | Na2SiO3 |
C | Cl2 | HCl | CuCl2 |
D | AlCl3 | Al(OH)3 | Al2O3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铜片、银片、Cu (NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池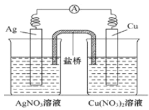 。以下有关该原电池的叙述正确的是( )
。以下有关该原电池的叙述正确的是( )
①在外电路中,电流由铜电极流向银电极
②正极反应为:Ag++e-=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
A.①②B.②③C.②④D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法正确的是( )

A. Mg 电极是该电池的正极
B. H2O2在石墨电极上发生氧化反应
C. 石墨电极附近溶液的pH 增大
D. 溶液中Cl-向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在有机物:①CH3CH3、②CH2=CH2、③CH3CH2C≡CH、④CH3C≡CCH3、⑤C2H6、⑥CH3CH=CH2中,一定互为同系物的是_______,一定互为同分异构体的是________________(填编号);
(2)以五倍子为原料可制得A,A结构简式为下图所示,回答下列问题:
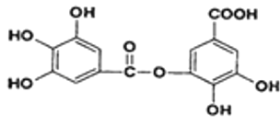
①A的分子式为______________;
②有机化合物B在硫酸催化条件下加热发生酯化可得到A。写出B的结构简式为_____ ;
(3)写出含有1个-CH2-、1个![]() 、3个-CH3原子团的烃类物质的结构简式___________;
、3个-CH3原子团的烃类物质的结构简式___________;
(4)写出核磁共振氢谱有两组峰,且峰面积之比为3:2,分子式为C8H10的芳香烃类化合物的结构简式_________;
(5)写出该有机物的名称![]() ________________。
________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com