
下列有关实验基本操作的说法错误的是( )
A.存放浓硝酸时,使用带玻璃塞的无色玻璃瓶
B.酸碱中和滴定时,若未用待测液润洗锥形瓶,对测定结果无影响
C.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗上口倒出
D.将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀
科目:高中化学 来源: 题型:
短周期元素A、B、C的原子序数依次递增,它们的原子最外层电子数之和为12,A与C同主族,B原子的最外层电子数等于A原子的次外层电子数,则下列叙述正确的是( )
A.原子半径:A<B<C
B.A的氢化物稳定性大于C的氢化物稳定性
C.三种元素的最高价氧化物对应水化物均可由化合反应得到
D.高温下,A单质能置换出C单质
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应A2(g)+2B2(g) 2AB2(g)△H <0,达到平衡后,改变条件,下列说法正确的是
2AB2(g)△H <0,达到平衡后,改变条件,下列说法正确的是
A.增加A2 的浓度,有利于该反应平衡逆向移动
B.升高温度有利于该反应平衡正向移动
C.升高温度,正向反应速率增加,逆向反应速率减小
D.增大压强有利于该反应平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
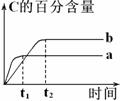
已知反应A(g)+B(g) nC(g) △H=x kJ·mol-1,在不同条件下进行时,混合物中C的百分含量随时间变化的关系如右图。下列有关叙述一定正确的是
nC(g) △H=x kJ·mol-1,在不同条件下进行时,混合物中C的百分含量随时间变化的关系如右图。下列有关叙述一定正确的是
A. a条件下的反应速率小于b条件下的反应速率
B. 其他条件相同时,a表示有催化剂,b表示无催化剂
C. 其他条件相同,若a、b表示不同压强下的反应,则n>2
D. 其他条件相同,若a、b表示不同温度下的反应,则x>0
查看答案和解析>>
科目:高中化学 来源: 题型:
已知一定温度和压强下,在起始容积为V L的容器中充入1 mol A和1 mol B,保持恒温恒压下反应:A(g)+B(g)  C(g) △H>0。达到平衡时,C的体积分数为40%。试回答:
C(g) △H>0。达到平衡时,C的体积分数为40%。试回答:
(1)升温时,C的反应速率 (填“加快”、“减慢”或“不变)。
(2)若使温度、压强在上述条件下恒定不变,平衡时在密闭容器中继续充入2 mol A和2 mol B,则反应再次达到平衡时,C的体积分数是
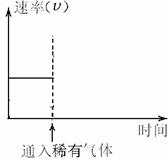
(3)若反应在恒温恒容条件下进行并达到平衡,保持其他条件不变,向容器中通入稀有气体,请在右图中画出通入稀有气体后的正逆反应速率随时间的变化图像,并标出v(正)、v(逆)及其关系。
查看答案和解析>>
科目:高中化学 来源: 题型:
下面所列的是中学化学实验室中几种常见的玻璃仪器:
①温度计 ②容量瓶 ③滴定管 ④烧杯 ⑤圆底烧瓶 ⑥量筒 ⑦玻璃棒
(1)在仪器上标明具体使用温度的是(不考虑温度计)________(填写编号);可作反应容器并可加热的是________(填写编号)。
(2)需要用温度计的实验是________(填写编号)。
①石油分馏 ②浓硫酸稀释 ③测定硝酸钾的溶解度
(3)玻璃棒的作用主要有以下三种。不同实验中其作用可能不完全相同,请回答下列问题:
①搅拌 ②引流 ③蘸取溶液
A.在“用无水碳酸钠配制100 mL 0.12 mol·L-1的碳酸钠溶液”的实验中,玻璃棒的作用是________(填写编号)。
B.在“用氢氧化钠溶液、碳酸钠溶液、氯化钡溶液、盐酸、水等试剂除去粗盐中的Mg2+、Ca2+、SO 等杂质离子以获得纯净的食盐”的实验中玻璃棒的作用可能是________(填写编号)。
等杂质离子以获得纯净的食盐”的实验中玻璃棒的作用可能是________(填写编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学为探究SO2与Ba2+只有在碱性条件下才能形成BaSO3沉淀,设计了如下方案,你认为可行的是( )
A.将SO2通入Ba(OH)2溶液中观察有白色沉淀生成
B.将SO2通入Ba(NO3)2溶液中观察有白色沉淀生成
C.将SO2分别通入BaCl2溶液、BaCl2与HCl的混合溶液、Ba(OH)2溶液中,观察到只有Ba(OH)2中有白色沉淀生成
D.将SO2通入BaCl2与NH3的混合溶液中有白色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
1丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125 ℃,反应装置如右图所示。下列对该实验的描述错误的是 ( )
A.不能用水浴加热
B.长导管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D.加入过量乙酸可以提高1-丁醇的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室里用二氧化锰与浓盐酸反应来制取适量的氯气,反应方程式为MnO2+4HCl(浓)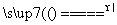 MnCl2+Cl2↑+2H2O。现用100 mL的浓盐酸与二氧化锰反应,生成的氯气在标准状况时的体积为5.6 L,计算:
MnCl2+Cl2↑+2H2O。现用100 mL的浓盐酸与二氧化锰反应,生成的氯气在标准状况时的体积为5.6 L,计算:
(1)用双线桥标出电子的转移。
(2)理论上需要参加反应的二氧化锰多少克?
(3)被氧化的HCl的质量为多少克?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com