
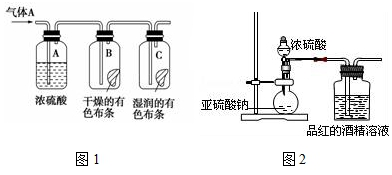
���� ��1���������Ա�ʵ��������ɫ������ʪ�����ɫ������������
��2��Ũ���������ˮ�Կ�����������ݸ��������������ʹ�������ɫ������ɫ��ʪ�����������ʹ��ɫ������ɫ��������
��3����������ˮ��Ӧ��Cl2+H2O=HCl+HClO��HClO���������ԣ�ǿ�����ԣ�Ư�����Լ����ȶ�����������
��1������ʵ��Ŀ�ļ�������������ʷ�������ȡ����������Ҷ��������ж���Ӧ��β������װ�ã�
��2�����ݶ��������ˮ��Ӧ�ķ���ʽ�жϣ�
��� �⣺��1����ʵ��ͨ���۲����������ʪ�����ֱ����ɫ������Ư�����ã����о������������û��Ư���ԣ�
�ʴ�Ϊ��̽��Cl2�ڳ�ʪ����ʱ�Ƿ����Ư���ԣ�
��2��Ũ������������������ˮ�ԣ���������������A�е�ˮ����������ͨ��Aƿ��Ũ������Bƿ�и���IJ�������ɫ��˵����������û��Ư���ԣ�Cƿ��������ˮ������ˮ����ɫ������ɫ��˵��ʪ��������ɫ������Ư�����ã�
��ΪB�ڵ���ɫ��������ɫ��C�ڵ���ɫ������ɫ��
�ʴ�Ϊ����������A�е�ˮ������B�ڵ���ɫ��������ɫ��C�ڵ���ɫ������ɫ��
��3��������ˮ����H+��HClO��HClO����ǿ�����ԣ�Ư���ԣ��ʿ�ʹ��ɫʯ����Һ�ȱ�����ɫ���ʴ�Ϊ��ʯ����Һ�ȱ�����ɫ��
��1����ʵ����̽�������SO2�ܲ���ʹƷ����ɫ�����Զ�������ͨ��Ʒ����ҺǰҪ���и�����������ж������Զ������岻��ֱ���ſգ���Ҫ��β������װ�ã�
�ʴ�Ϊ���ٶ�������û�и����ȱ�ٶ�������ĸ���װ�ã�����û��β������װ�ã�
��2�����������ˮ��Ӧ����������SO2+H2O?H2SO3��������Ʒ����ɫ�Ŀ�����H2SO3���ʴ�Ϊ��H2SO3��
���� ���⿼�����������ʼ�������ˮ��Ӧ�������Ư���ԣ���������������Լ�ʹƷ����ɫ��ԭ����Ŀ�ѶȲ���


 ѧ�ڸ�ϰһ��ͨѧϰ�ܶ�Ա��ĩ������ӱ����������ϵ�д�
ѧ�ڸ�ϰһ��ͨѧϰ�ܶ�Ա��ĩ������ӱ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH3CH2CH3 | B�� | CH3CH2CH2CH3 | C�� | CH3COCH2CH3 | D�� | 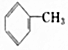 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
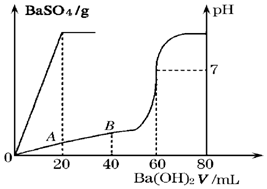 �����Dz�ͬ�¶���ˮ�����ӻ������ݣ�
�����Dz�ͬ�¶���ˮ�����ӻ������ݣ�| �¶�/�� | 25 | t1 | t2 |
| ˮ�����ӻ� | 1��10-14 | a | 1��10-12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| Ũ��mol/L | 4��10-6 | 6��10-6 | 2��10-5 | 4��10-5 | 3��10-5 | 2��10-5 |
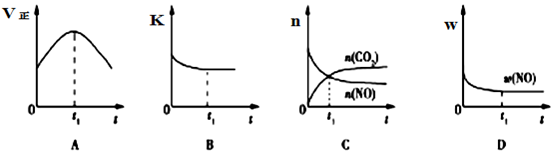
| ���� �¶�/�� | ����̿ | NO | E | F |
| ��ʼ | 3.000 | 0.10 | 0 | 0 |
| T1 | 2.960 | 0.020 | 0.040 | 0.040 |
| T2 | 2.975 | 0.050 | 0.025 | 0.025 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ҫʹ�ô�����ɳ����ʹ����½�ӵĺ�ɳ������ĺ�ɳ | |
| B�� | ���������ε�Ư���뺬����Ľ������ʹ�û�����ж����� | |
| C�� | Ư�ۺ�����������������ˮ�Ĵ��������ߵ����ú�ԭ������ͬ | |
| D�� | ��ɫ��ѧ�ĺ����Ǵ�Դͷ�ϼ��ٺ��������������Ի�������Ⱦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
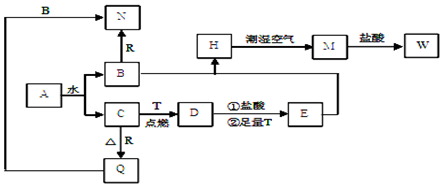

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
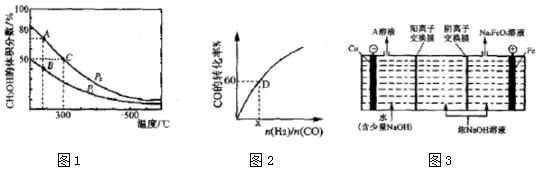
| ��Ӧ����v | ƽ�ⳣ��K | ƽ��ת���ʦ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
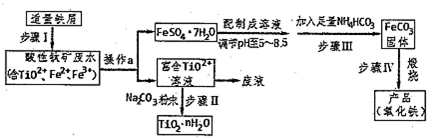
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com