
【题目】I.氮族元素包括N、P、As、Sb和Bi五种元素。
(1)下列关于氮族元素的说法正确的是_________。
a.N2可用于填充霓虹灯,其发光原理是电子从能量较低的轨道跃迁到能量较高的轨道时以光的形式释放能量
b.P、Na、S三种元素的第一电离能由大到小的顺序是:P>S>Na
c.基态As原子中,电子占据的最高能级为4d
d.Bi原子中最外层有5个能量相同的电子
(2)NH3在水中的溶解度比PH3大得多,其原因是_________。
向硫酸铜溶液中先加过量氨水,后加适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体,该晶体中不含有的化学键是_________。
Ⅱ.第四周期金属与人类的生产生活息息相关。
(3)目前市售的发光二极管,其材质以砷化镓(GaAs)为主。已知镓是与铝同族,镓的基态原子的电子排布式是_________。GaAs中Ga的化合价为_________。
(4)金属钛坚硬、强度大、耐热、密度小,被称为高技术金属。TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟,则TiCl4属于_________(填“原子”“分子”或“离子”)晶体。
(5)钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种的化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,产生白色沉淀;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为_________。
【答案】b 氨分子与水分子间能形成氢键 非极性键 1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1) +3 分子 [Co(NH3)5SO4]Br
【解析】
(1)a.只有当电子从能量较高的轨道跃迁到能量较低的轨道,才能以光的形式释放能量,从能量较低的轨道跃迁到能量较高的轨道时不释放能量,故错误;
b.同一周期元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于其相邻元素,所以P、Na、S三种元素的第一电离能由大到小的顺序是:P>S>Na,故正确;
c.基态As原子的核外电子排布式为1s22s22p63s23p63d104s24p3,电子占据的最高能级为4p,故错误;
d.Bi原子最外层电子排布式为5s25p3,s能级上电子能量相同,p能级上电子能量相同,故错误;
故答案为:b;
(2)氨分子和水分子之间易形成氢键,PH3和水分子不能形成氢键,氢键能增大氢化物的溶解性,所以NH3在水中的溶解度比PH3大得多;[Cu(NH3)4]SO4晶体为络合物,含有配位键、极性共价键和离子键,不含非极性键,故答案为:氨分子与水分子间能形成氢键;非极性键;
(3)镓与铝同族,位于周期表第4周期ⅢA族,原子序数为31,最外层有3个电子,最高正价为+3价,电子排布式为1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1),As的电负性大于Ga,则GaAs中As元素化合价为-3,Ga元素的化合价为+3,故答案为:1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1);+3;
(4)TiCl4在常温下是无色液体,熔沸点较低,说明TiCl4属于分子晶体,故答案为:分子;
(5)往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,说明不能电离出![]() ,
,![]() 为配离子,若加入AgNO3溶液时,产生淡黄色沉淀,说明电离出Br-,Br-为外界离子,则第二种配合物的化学式为[Co(NH3)5SO4]Br,故答案为:[Co(NH3)5SO4]Br。
为配离子,若加入AgNO3溶液时,产生淡黄色沉淀,说明电离出Br-,Br-为外界离子,则第二种配合物的化学式为[Co(NH3)5SO4]Br,故答案为:[Co(NH3)5SO4]Br。


科目:高中化学 来源: 题型:
【题目】用0.100 0molL﹣1 NaOH溶液滴定20.00mL未知浓度的盐酸(酚酞作指示剂)的滴定曲线如图所示.下列说法正确的是( )

A.水电离出的氢离子浓度:a>b
B.盐酸的物质的量浓度为0.0100 molL﹣1
C.指示剂变色时,说明盐酸与NaOH恰好完全反应
D.当滴加NaOH溶液10.00 mL(忽略反应前后体积变化),该混合液的pH=1+lg3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将镁片、铝片平行插入一定浓度的NaOH溶液中,用导线连成闭合回路,该装置在工作时,下列叙述中正确的是
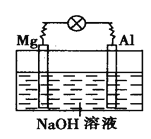
A. 镁比铝活泼,镁失去电子被氧化成Mg2+
B. 铝是电池的负极,开始工作时溶液中会立即有白色沉淀生成
C. 该装置的内、外电路中,均是电子的定向移动形成
D. 该装置开始工作时,铝片表面的氧化膜可不必处理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容积均为1L的甲、乙两个恒容容器中,分别充入2molA、2molB和1molA、1molB,相同条件下,发生下列反应:A(g)+B(g)![]() xC(g) △H<0。测得两容器中c(A)随时间t的变化如上图所示,下列说法不正确的是
xC(g) △H<0。测得两容器中c(A)随时间t的变化如上图所示,下列说法不正确的是

A.x=1
B.此条件下,该反应的平衡常数K=4
C.给乙容器升温可缩短反应达平衡的时间但不能提高平衡转化率
D.甲和乙的平衡转化率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物,单质铁、砷及它们的化合物广泛应用于超导体材料等领域,请回答下列问题:
(1)Fe2+的核外电子排布式为_________________。
(2)NH3是一种很好的配体,NH3的沸点______(填“>”“=”或“<”)AsH3。
(3)N原子核外有______种不同运动状态的电子。基态N原子中,能量最高的电子所占据的原子轨道的形状为___________。
(4)科学家通过X射线测得胆矾结构示意图可简单表示如图,图中虚线表示的作用力为________________。

(5)As的卤化物的熔点如下:
AsCl3 | AsBr3 | AsI3 | |
熔点/K | 256.8 | 304 | 413 |
表中卤化物熔点差异的原因是________________。
(6)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表Fe3+,则Fe3+与氮原子之间形成的化学键是_________,Fe3+的配位数为_________。

(7)FeS2晶体的晶胞如图所示。晶胞边长为anm、FeS2相对式量为M、阿伏加德罗常数的值为NA,其晶体密度的计算表达式为_________g·cm-3;晶胞中Fe2+位于S22-所形成的正八面体的体心,该正八面体的边长为_________nm。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,只改变反应物中n(SO2)对反应2SO2(g)+O2(g)2SO3(g)的影响如图所示,下列说法正确的是( )
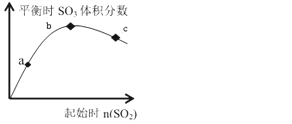
A. 反应a、b、c点均为平衡点,且b点时SO2的转化率最高
B. b点时SO2与O2 的物质的之比约为2:1
C. a、b、c 三点平衡常数: Kb>Kc>Ka
D. a、b、c 三点反应速率大小为: vb>vc>va
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒温恒压的密闭容器中发生如下反应:A(g)+B(g)2C(g) △H<0,t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图所示。下列说法不正确的是( )

A.0~t2时,v(正)>v(逆)
B.Ⅰ、Ⅱ两过程达到平衡时,A的体积分数Ⅰ=Ⅱ
C.t2时刻改变的条件是向密闭容器中加C
D.Ⅰ、Ⅱ两过程达到平衡时,平衡常数K(Ⅰ)=K(Ⅱ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容积均为1L的甲、乙两个恒容容器中,分别充入2molA、2molB和1molA、1molB,相同条件下,发生下列反应:A(g)+B(g)![]() xC(g) △H<0。测得两容器中c(A)随时间t的变化如上图所示,下列说法不正确的是
xC(g) △H<0。测得两容器中c(A)随时间t的变化如上图所示,下列说法不正确的是
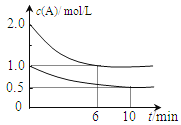
A.x=1
B.此条件下,该反应的平衡常数K=4
C.给乙容器升温可缩短反应达平衡的时间但不能提高平衡转化率
D.甲和乙的平衡转化率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,pH=12的氢氧化钠和pH=4的醋酸等体积混合后恰好中和,忽略混合后溶液体积的变化,下列说法中正确的是
A.混合后的溶液呈中性B.混合前两溶液中水的电离程度不同
C.氢氧化钠和醋酸的浓度不相等D.混合前的醋酸约1%发生电离
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com