
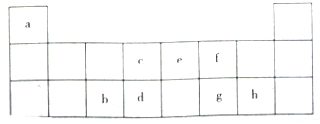
 如该表是元素周期表的短周期部分,表中字母分别表示一种元素.请回答下列问题:
如该表是元素周期表的短周期部分,表中字母分别表示一种元素.请回答下列问题: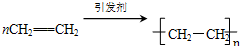 ;
;分析 根据元素所在周期表中的位置可知a为H元素,b为Al元素,c为C元素,d为Si元素,e为N元素,f为O元素,g为S元素,h为Cl元素,结合元素周期律的递变规律以及对应物质的性质进行分析.
解答 解:根据元素所在周期表中的位置可知a为H元素,b为Al元素,c为C元素,d为Si元素,e为N元素,f为O元素,g为S元素,h为Cl元素,
(1)HClO4是酸性最强的无机含氧酸,
故答案为:HClO4;
(2)非金属性越强氢化物越稳定,由元素在周期表的位置可知,非金属性Si<N<O,故氢化物稳定性SiH4<NH3<H2O,
故答案为:SiH4<NH3<H2O;
(3)H、C两种元素可形成多种化合物,化合物A的产量是衡量一个国家石油化工发展水平的标志,则A为乙烯,
①A的结构简式为CH2=CH2,乙烯发生加聚反应得到聚乙烯,方程式为: ,
,
故答案为:CH2=CH2; ;
;
②乙烯与水发生加成反应生成的B,B为CH3CH2OH,以乙酸反应生成乙酸乙酯,方程式为:CH3COOH+CH3CH2OH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,
故答案为:加成反应;CH3COOH+CH3CH2OH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
(4)元素e的气态氢化物与其最高价氧化物的水化物反应生成的物质为NH4NO3,属于离子化合物,含有离子键、共价键,
故答案为:NH4NO3;离子键、共价键;离子.
点评 本题考查结构性质位置关系、元素周期律、有机物的推断与性质、元素化合物性质等,难度不大,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体粒子的大小通常在0.1~1nm之间 | |
| B. | 阳光穿透清晨的树林时形成的光柱,是胶体的丁达尔效应的体现 | |
| C. | 可以通过过滤分离溶液和胶体 | |
| D. | 向FeCl3溶液中加入NaOH溶液,会出现红褐色Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤ | B. | ④⑤⑦ | C. | ①③④⑤ | D. | ④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{4M}{{a}^{3}}$ | B. | $\frac{M}{{a}^{3}{N}_{A}}$ | C. | $\frac{2M}{{a}^{3}{N}_{A}}$ | D. | $\frac{4M}{{a}^{3}{N}_{A}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.4 mol | B. | 4 mol | C. | 2.8 mol | D. | 1.2 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com