
【题目】碳碳双键不能自由转动,所以R—CH==CH—R可有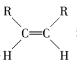 和
和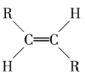 两种空间排列形式,判断下列化合物中具有上述两种空间排列形式的是
两种空间排列形式,判断下列化合物中具有上述两种空间排列形式的是
A.丙烯B.氯乙烯C.2-戊烯D.苯乙烯
【答案】C
【解析】
根据信息进行如果连接双键的碳原子上含有两个不同的基团时,该有机物有两只空间排列形式,据此分析。
A. 丙烯的结构简式为CH2=CH-CH3,双键的左边碳原子上含有两个相同的原子,因此丙烯只有一种排列形式,故A不符合题意;
B. 氯乙烯的结构简式为CH2=CHCl,双键左边碳原子上含有两个相同的原子,氯乙烯只有一种排列形式,故B不符合题意;
C. 2-戊烯的结构简式为CH3CH=CHCH2CH3,连接双键的两个碳原子上都含有两个不同的基团,因此2-戊烯具有两种空间排列方式,故C符合题意;
D. 苯乙烯的结构简式为![]() ,双键的右边碳原子上含有两个相同的原子,因此苯乙烯只有一种空间排列方式,故D不符合题意;
,双键的右边碳原子上含有两个相同的原子,因此苯乙烯只有一种空间排列方式,故D不符合题意;
答案:C。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】某温度下,![]() 。向物质的量浓度相同的
。向物质的量浓度相同的![]() 和
和![]() 的混合溶液中滴加
的混合溶液中滴加![]() 溶液产生
溶液产生![]() 、
、![]() 两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。
两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。
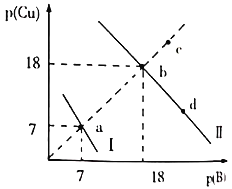
图中的![]() ,
,![]() 或
或![]() 。下列说法错误的是( )
。下列说法错误的是( )
A.曲线Ⅰ表示的是Cu2+与OH-浓度关系的曲线
B.该温度下,![]()
C.升高温度时,b点会向c点移动
D.向d点对应的溶液中加入对应阴离子的钠盐固体,d点向b点移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为一定条件下采用多孔惰性电极的储氢电池充电装置(忽略其他有机物)。已知储氢装置的电流效率![]() ×100%,下列说法不正确的是
×100%,下列说法不正确的是
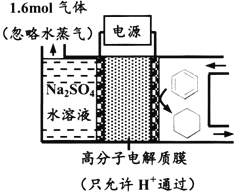
A. 采用多孔电极增大了接触面积,可降低电池能量损失
B. 过程中通过C-H键的断裂实现氢的储存
C. 生成目标产物的电极反应式为C6H6+6e-+6H+===C6H12
D. 若![]() =75%,则参加反应的苯为0.8mol
=75%,则参加反应的苯为0.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A.11g的D218O中含有的中子数为5NA
B.1 LpH=2的H2SO4溶液中H+的数目为0. 02NA
C.将0.1mol Cl2通入足量FeI2溶液中,转移电子的数目为0.2NA
D.标准状况下,4. 48 L甲烷与足量Cl2完全反应生成CH3Cl的分子数目为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)(填序号)下列实验操作或对实验事实的叙述正确的是______。
①用稀HNO3清洗做过银镜反应实验的试管
②配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌
③用碱式滴定管量取20.00 mL 0.1000 mol·L-1KMnO4溶液
④用托盘天平称取10.50 g干燥的NaCl固体
⑤不慎将苯酚溶液沾到皮肤上,立即用酒精清洗
⑥用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物
⑦向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体
⑧配制Al2(SO4)3溶液时,加入少量的稀硫酸
(2)为了确定乙醇分子的结构简式是CH3—O—CH3还是CH3CH2OH,实验室利用如图所示的实验装置,测定乙醇与钠反应(ΔH<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目。试完成下列问题:
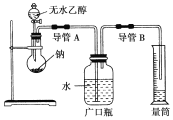
指出实验装置中的错误________。
②若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得的氢气体积将______(填“偏大”、“偏小”或“不变”)。
③请指出能使该实验安全、顺利进行的关键实验步骤________________(至少指出两个关键步骤)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】思维辨析:
(1) 互为同分异构体。_________
互为同分异构体。_________
(2)烯烃分子中所有原子都在同一平面上_________
(3)既可以用溴水鉴别甲烷和乙烯,又可以用溴水除去甲烷中的乙烯。_________
(4)煤中含有芳香烃,可以通过干馏的方法得到芳香烃。_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用系统命名法命名烃A:_______________________________;
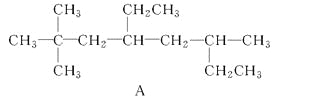
烃A的一氯代物具有不同沸点的产物有________种。
(2)有机物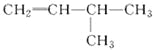 的系统名称是______________,将其在催化剂存在下完全氢化,所得烷烃的系统名称是__________________。
的系统名称是______________,将其在催化剂存在下完全氢化,所得烷烃的系统名称是__________________。
(3)有机物![]() 的系统名称是______________,将其在催化剂存在下完全氢化,所得烷烃的系统名称是__________________。
的系统名称是______________,将其在催化剂存在下完全氢化,所得烷烃的系统名称是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):

H2SO4(浓)+NaBr ![]() NaHSO4+HBr↑
NaHSO4+HBr↑
CH3CH2OH+HBr![]() CH3CH2Br+H2O。有关数据见下表:
CH3CH2Br+H2O。有关数据见下表:
乙醇 | 溴乙烷 | 溴 | |
状态 | 无色液体 | 无色液体 | 深红色液体 |
密度/(g·cm-3) | 0.79 | 1.44 | 3.1 |
沸点/℃ | 78.5 | 38.4 | 59 |
(1)A装置的名称是______________。
(2)实验中用滴液漏斗代替分液漏斗的优点为_______________________。
(3)给A加热温度过高或浓硫酸的浓度过大,均会使C中收集到的粗产品呈橙色,原因是A中发生了副反应,写出此反应的化学方程式________________________。
(4)给A加热的目的是________________________,F接橡皮管导入稀NaOH溶液,其目的主要是___________________。
(5)图中C中的导管E的末端须在水面以下,其目的是______________________。
(6)粗产品洗涤、分液后,再经过蒸馏水洗涤、分液,然后加入少量的无水硫酸镁固体,静置片刻后过滤,再将所得滤液进行蒸馏,收集到的馏分约10.0 g。从乙醇的角度考虑,本实验所得溴乙烷的产率是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B. [实验化学]
乙酰苯胺具有退热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称。其制备原理如下:

已知:
①苯胺易被氧化;
②乙酰苯胺、苯胺和醋酸的部分物理性质如下表:
物质 | 熔点 | 沸点 | 溶解度(20 ℃) |
乙酰苯胺 | 114.3℃ | 305℃ | 0.46 |
苯胺 | -6℃ | 184.4℃ | 3.4 |
醋酸 | 16.6℃ | 118℃ | 易溶 |
实验步骤如下:
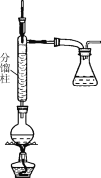
步骤1:在50 mL圆底烧瓶中,加入5 mL苯胺、7.5 mL冰醋酸及少许锌粉,依照如图装置组装仪器。
步骤2:控制温度计示数约105 ℃,小火加热回流1 h。
步骤3:趁热将反应混合物倒入盛有100 mL冷水的烧杯中,冷却后抽滤,洗涤,得到粗产品。
(1)步骤1中加入锌粉的作用是________。
(2)步骤2中控制温度计示数约105℃的原因是________。
(3)步骤3中趁热将混合物倒入盛有冷水的烧杯中,“趁热”的原因是__________________。抽滤装置所包含的仪器除减压系统外,还有________、________(填仪器名称)。
(4)步骤3得到的粗产品需进一步提纯,该提纯方法是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com