
| A.Fe:1s22s22p63s23p63d54s3 | B.F ˉ:1s22s22p6 |
| C.K:1s22s22p63s23p64s1 | D.Kr:1s22s22p63s23p63d104s24p6 |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ①Z的原子序数为29,其余的均为短周期主族元素;
①Z的原子序数为29,其余的均为短周期主族元素; ②Y原子价电子(外围电子)排布msnmpn
②Y原子价电子(外围电子)排布msnmpn  ③R原子核外L层电子数为奇数;
③R原子核外L层电子数为奇数; ④Q、X原子p轨道的电子数分别为2和4。
④Q、X原子p轨道的电子数分别为2和4。 请回答下列问题:
请回答下列问题: (1)Z2+ 的核外电子排布式是 ,Z原子基态时简化电子排布式为 。
(1)Z2+ 的核外电子排布式是 ,Z原子基态时简化电子排布式为 。 (2)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是 。
(2)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是 。
| A.稳定性:甲>乙,沸点:甲>乙 | B.稳定性:甲>乙,沸点:甲<乙 | C.稳定性:甲<乙,沸点:甲<乙 | D.稳定性:甲<乙,沸点:甲>乙 |
 (3)Q、R、Y三种元素的第一电离能数值由小到大的顺序为 (用元素符号作答)。
(3)Q、R、Y三种元素的第一电离能数值由小到大的顺序为 (用元素符号作答)。 (4)五种元素中,电负性最大与最小的两种非金属元素形成的化合物的化学式为 。
(4)五种元素中,电负性最大与最小的两种非金属元素形成的化合物的化学式为 。 (5)Q的一种氢化物相对分子质量为28,其中分子中的σ键与π键的键数之比为 ,该氢化物与氧气形成的燃料电池在碱性电解质中负极反应为 。
(5)Q的一种氢化物相对分子质量为28,其中分子中的σ键与π键的键数之比为 ,该氢化物与氧气形成的燃料电池在碱性电解质中负极反应为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
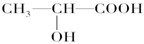
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.最外层有6个电子 |
| B.位于元素周期表的第七周期 |
| C.主要化合价为-4价、+4价 |
| D.电解硝酸铜与硝酸“类铅”的混合溶液时首先会析出“类铅” |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
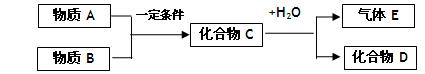
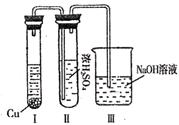
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 B、C、D的原子序数都小于18,A与D同主族,B与C在同一周期,A、D原子的最外层电子数都是1,C原子最外层电子数比B原子少2个,且C最外层电子数是次外层电子数的2倍。A、B单质在常温下均为气体,它们在高温下以体积比2∶1完全反应,生成物在常温下是液体。此液体与D单质能激烈反应生成A的单质。所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的阳离子。回答下列问题:
B、C、D的原子序数都小于18,A与D同主族,B与C在同一周期,A、D原子的最外层电子数都是1,C原子最外层电子数比B原子少2个,且C最外层电子数是次外层电子数的2倍。A、B单质在常温下均为气体,它们在高温下以体积比2∶1完全反应,生成物在常温下是液体。此液体与D单质能激烈反应生成A的单质。所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的阳离子。回答下列问题:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
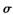 键和
键和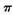 键个数之比为____________。
键个数之比为____________。
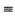 Y放出942KJ热量。试写出由Y4气态分子变成Y2气态分子的热化学方程式___
Y放出942KJ热量。试写出由Y4气态分子变成Y2气态分子的热化学方程式___ _____________________
_____________________查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com