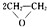(2008?揭阳一模)2007年3月,温家宝总理在十届人大五次会议上指出要大力抓好节能降耗、保护环境.请你分析并回答下列问题:
(1)“绿色化学”的最大特点在于它是在始端就采用预防实际污染的科学手段,因而过程和终端均为零排放和零污染,具有“原子经济性”.下列化学反应不符合“绿色化学”思想的是
BD
BD
.
A.制备环氧乙烷:2CH
2=CH
2+O
2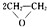
B.制备硫酸铜:Cu+2H
2SO
4 CuSO
4+SO
2↑+2H
2O
C.制备甲醇:2CH
4+O
2 2CH
3OH
D.制备硝酸铜:3Cu+8HNO
3(稀)=3Cu(NO
3)
2+2NO↑+4H
2O
(2)冶金废水中含有[Au(CN)
2]
-,其电离出的CN
-有毒,当与H
+结合生成HCN时,其毒性更强.工业上处理这种废水是在碱性条件下,用NaClO将CN
-氧化为CO
32-和一种无毒气体,该反应的方程式为
5ClO-+2CN-+2OH-=2CO32-+N2↑+5Cl-+H2O
5ClO-+2CN-+2OH-=2CO32-+N2↑+5Cl-+H2O
,在酸性条件下,ClO
-也能将CN
-氧化,但实际处理时却不在酸性条件下进行的主要原因是
在酸性条件下,CN-与H+结合生成毒性很强的HCN,对人和环境造成危害
在酸性条件下,CN-与H+结合生成毒性很强的HCN,对人和环境造成危害
.
(3)工业上目前使用两种方法制取乙醛--“乙炔水化法”和“乙烯氧化法”.下面两表提供生产过程中原料、反应条件、原料平衡转化率和产量等的有关信息:
|
乙炔水化法 |
乙烯氧化法 |
| 原料 |
乙炔、水 |
乙烯、空气 |
| 反应条件 |
HgSO4、100~125℃ |
PdCl2-CuCl2、100~125℃ |
| 平衡转化率 |
乙炔平衡转化率90%左右 |
乙烯平衡转化率80%左右 |
| 日产量 |
2.5吨(某设备条件下) |
3.6吨(相同设备条件下) |
表一:原料、反应条件、平衡转化率、日产量
表二:原料来源生产工艺
|
原料生产工艺过程 |
| 乙炔 |
CaCO3CaOCaC2C2H2 |
| 乙烯 |
来源于石油裂解气 |
从两表中分析,现代工业上“乙烯氧化法”将逐步取代“乙炔水化法”的可能原因.
①从产率和产量角度分析
虽然乙烯氧化法的转化率略小于乙炔水化法,但反应快、日产量比其高得多
虽然乙烯氧化法的转化率略小于乙炔水化法,但反应快、日产量比其高得多
.
②从环境保护和能耗角度分析
两者反应条件温度相当,但乙炔水化法制乙醛使用的是汞盐催化剂,毒性大;乙炔的制取要经过多步反应制得,且消耗大量的热能、电能;乙烯来源于石油裂解气,消耗的总能量比乙炔少,且较容易获得
两者反应条件温度相当,但乙炔水化法制乙醛使用的是汞盐催化剂,毒性大;乙炔的制取要经过多步反应制得,且消耗大量的热能、电能;乙烯来源于石油裂解气,消耗的总能量比乙炔少,且较容易获得
.

 名校课堂系列答案
名校课堂系列答案