
| A. | 在Na2SO4溶液中,c(Na+):c(SO42-) | |
| B. | 相同温度下,0.2 mol/L CH3COOH溶液中c(H+)与0.1 mol/LCH3COOH溶液中c(H+) | |
| C. | 在密闭容器中,反应N2(g)+3H2(g)?2NH3 (g)已达平衡时的c(NH3)与c(N2) | |
| D. | 液面均在“0”刻度时,50mL碱式滴定管和25mL碱式滴定管所盛溶液体积 |
分析 A.Na2SO4溶液中,钠离子和硫酸根离子都不水解,结合硫酸钠的化学式判断c(Na+):c(SO42-);
B.醋酸的浓度大小影响醋酸的电离程度,浓度越大醋酸的电离程度越小;
C.没有告诉氨气与氮气的浓度关系,无法判断c(NH3):c(N2)的比值;
D.滴定管最大数值下面还有溶液,其体积未知.
解答 解:A.在Na2SO4溶液中,Na+和SO42-都不水解,则硫酸钠溶液中c(Na+):c(SO42-)=2:1,故A正确;
B.相同温度下,0.2 mol/L CH3COOH溶液中c(H+)与0.1 mol/LCH3COOH溶液中c(H+),前者溶液中醋酸的电离程度小于后者,则前者溶液中的氢离子浓度小于后者的2倍,故B错误;
C.在密闭容器中,由于氮气和氨气的浓度未知,无法计算反应N2(g)+3H2(g)?2NH3(g)已达平衡时c(NH3)与c(N2)的比值,故C错误;
D.滴定管最大值下面还有溶液,且这部分溶液的体积未知,导致无法计算其溶液体积的比值,故D错误;
故选A.
点评 本题考查了可逆反应特点、弱电解质的电离、滴定管构造等知识,题目难度中等,明确弱电解质的电离平衡、可逆反应特点为解答关键,试题培养了学生的灵活应用能力.


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 石油中含有C5~C11的烷烃,可以通过石油的分馏得到汽油 | |
| B. | 含C18以上烷烃的重油经过催化裂化得到汽油 | |
| C. | 石油的裂解是化学变化,石油的分馏是物理变化 | |
| D. | 石油裂解气的主要成分是各种烯烃,并不含有烷烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{1}^{1}$H和${\;}_{1}^{2}$H | B. | 金刚石和石墨 | ||
| C. | CH3CH2OH和CH3OCH3 | D. | CH4和C2H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
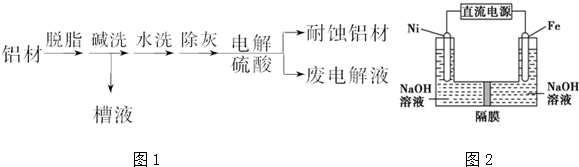
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3+3CO=═2Fe+3CO2△H=-28.5 kJ•mol-1 | |
| B. | Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-28.5 kJ | |
| C. | Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=+28.5 kJ•mol-1 | |
| D. | Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-28.5 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
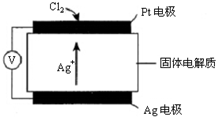 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱,以及生产ClO2和氯的含氧酸盐(NaClO、NaClO3)等系列化工产品.
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱,以及生产ClO2和氯的含氧酸盐(NaClO、NaClO3)等系列化工产品.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PO43- | B. | CCl4 | C. | NO3- | D. | SiH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCO3═CaO+CO2↑ | B. | NaHCO3+NaOH═Na2CO3+H2O | ||
| C. | Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO | D. | 3K2MnO4+2H2O═2KMnO4+MnO2↓+4KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com