
| A. | ①②④ | B. | ①②③④ | C. | ①②③ | D. | ①③④ |
分析 ①若甲为氨气,则丁可能是O2,乙为NO,丙为NO2,符合转化关系;
②若丁是氢氧化钠溶液,甲可能是一种能使品红溶液褪色的气体,甲为SO2,乙为NaHSO3,丙为Na2SO3;
③若甲为碳,丁为O2,乙为CO,丙为CO2,碳与二氧化碳可以反应生成CO;
④若甲为硝酸银溶液,丁可以为氨气,乙为AgOH,丙为[Ag(NH3)2]OH.
解答 解:①若甲为氨气,则丁可能是O2,乙为NO,丙为NO2,符合转化关系,故正确;
②若丁是氢氧化钠溶液,甲可能是一种能使品红溶液褪色的气体,甲为SO2,乙为NaHSO3,丙为Na2SO3,符合转化关系,故正确;
③若甲为碳,丁为O2,乙为CO,丙为CO2,碳与二氧化碳可以反应生成CO,符合转化关系,故正确;
④若甲为硝酸银溶液,丁可以为氨气,乙为AgOH,丙为[Ag(NH3)2]OH,符合转化关系,故正确,
故选:B.
点评 本题考查无机物推断,关键是熟练掌握元素化合物性质与转化,掌握中学常见连续反应.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
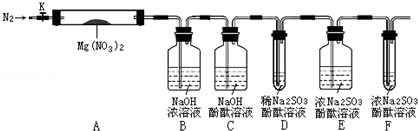
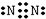 ,步骤Ⅱ中,通入一段时间N2的目的是避免对分解产物O2的检验产生干扰.
,步骤Ⅱ中,通入一段时间N2的目的是避免对分解产物O2的检验产生干扰.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将稀硫酸改成浓硫酸 | B. | 滴加少量硫酸钠溶液 | ||
| C. | 硫酸改成4 mol•L-1的醋酸 | D. | 滴加几滴硫酸铜溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径大小关系为Z>Y>X | |
| B. | 由X、Z、M、W四种元素形成的化合物都不能用于焙制糕点的食品工业 | |
| C. | 由X、Y、Z、M四种元素形成的所有化合物既能和强酸反应又能和强碱反应 | |
| D. | 由X与M形成的不同分子的空间构型可能是正四面体型、直线型或平面型等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
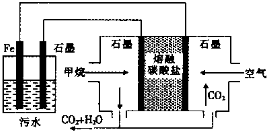
| A. | 左侧装置中的铁电极可换成石墨电极 | |
| B. | 通入甲烷的石墨电极的电极反应式为:CH4+4CO32--8e-═5CO2+2H2O | |
| C. | 通入空气的石墨电极做正极,发生氧化反应 | |
| D. | 若左侧装置中石墨电极产生标准状况下气体44.8L气体,则消耗2mol甲烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 决定某化学反应反应速率的主要因素是催化剂 | |
| B. | 青霉素、橡胶、阿斯匹林全部由化学合成制得 | |
| C. | 铝有还原性,在反应中放出大量热能用来冶炼难熔金属Mn等 | |
| D. | 陶瓷品、酒精、乙烯塑料等的使用不会对环境造成污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、蒸馏、萃取 | B. | 萃取、蒸发、分液 | C. | 分液、萃取、蒸馏 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com