

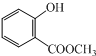
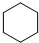
分析 (1)只含C、H两种元素的有机物叫做烃,烃的不饱和度越高,碳质量分数最高;
(2)分子式相同,但结构不同的化合物互为同分异构体,结构相似,分子组成上相差一个或若干个CH2的化合物,互为同系物;
(3)③中苯环上的碳原子和烯基上的碳原子都是sp2 杂化,1mol⑧中含有σ键的物质的量为C-Hσ键是6×2=12mol,C-Cσ键是6mol,共18mol;
(4)⑤中位于同一平面上碳原子可能是任意两个苯环和中心的一个碳原子,所以最多为6×2+1=13;
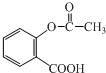
(5) 中的酚酯消耗2mol的氢氧化钠、羧基消耗1mol的氢氧化钠,由此分析解答.
中的酚酯消耗2mol的氢氧化钠、羧基消耗1mol的氢氧化钠,由此分析解答.
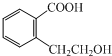
解答 解:(1)在① ;②
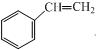
;② ;③
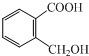
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ ;⑧
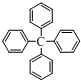
;⑧ 中①③⑤⑧是烃,其不饱和度分别为:2、5、16、1,所以属于烃,且含碳质量分数最高的是⑤,故答案为:⑤;
中①③⑤⑧是烃,其不饱和度分别为:2、5、16、1,所以属于烃,且含碳质量分数最高的是⑤,故答案为:⑤;
(2)分子式相同,但结构不同的化合物互为同分异构体,所以④⑥是同分异构体,结构相似,分子组成上相差一个或若干个CH2的化合物,互为同系物,②④是同系物,故答案为:④⑥;②④;
(3))③中苯环上的碳原子和烯基上的碳原子都是sp2 杂化,1mol⑧中含有σ键的物质的量为C-Hσ键是6×2=12mol,C-Cσ键是6mol,共18mol,故答案为:sp2;18;
(4) 中位于同一平面上碳原子可能是任意两个苯环和中心的一个碳原子,所以最多为6×2+1=13,故答案为:13;
中位于同一平面上碳原子可能是任意两个苯环和中心的一个碳原子,所以最多为6×2+1=13,故答案为:13;
(5) 中的酚酯消耗2mol的氢氧化钠、羧基消耗1mol的氢氧化钠,所以共消耗3mol的氢氧化钠,故答案为:3.
中的酚酯消耗2mol的氢氧化钠、羧基消耗1mol的氢氧化钠,所以共消耗3mol的氢氧化钠,故答案为:3.
点评 本题考查烃概念、有机物的不饱和度、碳原子的杂化方式、共价键的类型、共平面的问题和酯和羧酸与碱的反应,综合性强,有一定的难度.


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:填空题
(1)发射卫星的火箭推进器中大多使用燃料偏二甲肼,其化学式C2H8N2。用NA表示阿伏加德罗常数的数值,试计算:
①偏二甲肼的摩尔质量是____________。
②偏二甲肼中碳原子与氮原子物质的量之比是____________;1 mol偏二甲肼中含有的氢原子数目是________________。
(2)据报道,加利福尼亚大学的科研人员发现了世界上最强的酸。这种强酸的化学式是CHB11Cl11。其中l1个硼原子和1个碳原子排列成20面体,这是目前化合物中化学性质最为稳定的原子组合。请回答下列问题:
①这种超强酸由____________种元素组成。
②1mol该超强酸中含有的氯原子数目为___________,若称取该超强酸1049g,则其中含硼原子的数目为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10个 | B. | 20个 | C. | 40个 | D. | 80 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
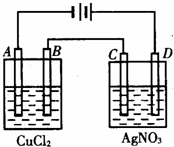 如图为以惰性电极进行电解:
如图为以惰性电极进行电解:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com