
把3molP和2.5molQ置于2L密闭容器中发生如下反应:3P(g)+Q(g)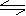 xM(g)+2N(g)经5mim反应达平衡时,测知生成1molN,M的平均反应速率为0.1mol/(L.min),下列叙述错误的是
xM(g)+2N(g)经5mim反应达平衡时,测知生成1molN,M的平均反应速率为0.1mol/(L.min),下列叙述错误的是
A.P的平均反应速率为0.15 mol/(L.min);
B.Q的转化率为25%;
C.Q的平衡浓度为1mol/L;
D.x的值是2。
B
【解析】
试题分析: 3P(g)+ Q(g)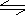 xM(g)+2N(g)
xM(g)+2N(g)
开始物质的量 3 2.5 0 0
变化物质的量 1.5 0.5 1
平衡物质的量 1.5 2 1
A.已知达到平衡生成1molN,则参加反应的P为n(P)=3/2×1mol=1.5mol,所以v(P)=1.5/(2x5) =0.15 mol/(L?min),A正确;B.已知达到平衡生成1molN,则参加反应的Q为n(Q)=1/2n(N)=0.5mol,所以Q的转化率为:0.5/2.5×100% =20%,B错误;C.参加反应的Q为n(Q)=1/2n(N)=0.5mol,故Q的平衡浓度为2/2=1mol/L,C正确;D.根据A选项可知v(P)=0.15 mol/(L?min),而M的平均速率是0.1mol/(L?min),根据速率之比等于化学计量数之比,则x/3=0.1/0.15,所以x=2,D正确,选B。
考点:考查化学反应速率的有关计算。


科目:高中化学 来源:2014-2015学年河南省高一上第二次考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列说法中正确的是( )。
A.1NA个氢气分子所占的体积为22.4 L
B.2NA个二氧化碳分子的质量为88 g
C.0.1 mol/L 的NaCl溶液中,Na+与Cl-离子总数为0.2NA
D.17 g NH3中所含原子数为NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高一上学期期中化学试卷(解析版) 题型:选择题
下列各组中的离子,能在溶液中大量共存的是
A.Na+、H+、SO42-、OH-
B.K+、Ca2+、CO32-、NO3-
C.Na+、H+、Cl-、CO32-
D.K+、Cu2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省洛阳市高二10月月考化学试卷(解析版) 题型:填空题
(1)工业制氢气的一个重要反应是:CO(g)+ H2O(g) == CO2(g) + H2(g)
已知25℃时:C(石墨) +O2 (g) == CO2(g) △H1 =-394 kJ·mol-1
C(石墨) +1/2O2 (g) == CO (g) △H2 =-111 kJ·mol-1
H2(g) +1/2O2 (g)== H2O(g) △H3=-242kJ·mol-1
试计算25℃时CO(g)+ H2O(g) == CO2(g) + H2(g)的反应热______kJ·mol-1
(2)830K时,在密闭容器中发生下列可逆反应:
CO(g)+H2O(g)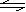 CO2(g)+H2(g);△H<0 试回答下列问题:
CO2(g)+H2(g);△H<0 试回答下列问题:
①若起始时c(CO)=2 mol·L-1,c(H2O)=3 mol·L-1,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K= .
②在相同温度下,若起始时c(CO)=1 mol·L-1,c(H2O)=2 mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,则此时该反应是否达到平衡状态 (填“是”与“否”),此时v(正) v(逆)(填“大于”“小于”或“等于”),你判断的依据是
③若降低温度,该反应的K值将 ,该反应的化学反应速率将 (均填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省洛阳市高二10月月考化学试卷(解析版) 题型:选择题
可逆反应:3R(气) 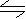 3M(?)十N(?) ( 吸热反应 ),随着温度的升高,气体平均相对分子质量有变小的趋势。则下列判断中正确的是( )
3M(?)十N(?) ( 吸热反应 ),随着温度的升高,气体平均相对分子质量有变小的趋势。则下列判断中正确的是( )
A.M和N可能都是固体 B.若N为固体.则M一定是气体
C.M和N一定都是气体 D.若M为固体.则N一定是气体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省洛阳市高二10月月考化学试卷(解析版) 题型:选择题
在温度和容积不变的容器中,一定条件下发生下列变化:H2(g)  2H(g)(气态氢原子)。ΔH >0。当容器中H2的浓度从0.1mol/L变为0.06mol/L时,需20秒,那么H2的浓度由0.06mol/L下降到0.036mol/l时需时间:( )
2H(g)(气态氢原子)。ΔH >0。当容器中H2的浓度从0.1mol/L变为0.06mol/L时,需20秒,那么H2的浓度由0.06mol/L下降到0.036mol/l时需时间:( )
A.12秒 B.无法判断 C.大于12秒 D. 小于12秒
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省洛阳市高一10月月考化学试卷(解析版) 题型:填空题
将标准状况下22.4 L的HCl溶于水配成200 mL的溶液,所得溶液的物质的量浓度为_____mol/L;配制300 mL 0.5 mol·L-1氯化钠溶液,需要1.5 mol·L-1的氯化钠溶液的体积是________mL。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省汝州市高二上学期第一次月考化学试卷(解析版) 题型:填空题
已知NO2和N2O4可以相互转化:N2O4(g) 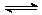 2NO2(g) △H<0,现将一定量NO2和N2O4的混合气体,通入体积为1L的恒温密闭容器中,各物质浓度随时间变化关系如下图所示:
2NO2(g) △H<0,现将一定量NO2和N2O4的混合气体,通入体积为1L的恒温密闭容器中,各物质浓度随时间变化关系如下图所示:

(1)图中共有两条曲线X和Y,其中表示N2O4浓度 随时间变化的曲线是_________
(2)前10min内,v(N2O4)= ______________ ;
(3)a、b、c、d四个点中,表示化学反应处于平衡状态的是____,此时反应的平衡常数为______________(只要求写数值)
(4)反应进行到25min时,曲线发生变化的原因是____________________________;
若要达到最后相同的化学平衡状态,在25min时还可以采取的措施是( )(双选)
A.升高温度 B.缩小容器体积 C.加入催化剂 D.加入一定量的N2O4
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省西区高一9月月考化学试卷(解析版) 题型:选择题
已知乙酸乙酯(C4H8O2)是一种无色液体,不溶于水,密度小于1 g·mL-1,沸点约为55 ℃。要从水与乙酸乙酯的混合物中将乙酸乙酯分离出来,下列方法中最简便的是( )
A.蒸馏 B.分液 C.过滤 D.蒸发
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com