
有无色溶液,加入Na2O2时有无色无味气体放出,并有白色沉淀生成,加入Na2O2的量与生成白色沉淀的量如图所示.该无色溶液中含有的物质是()
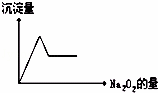
| A. | CaCl2和MgCl2、 | B. | Al2 (SO4)3 | |
| C. | Al2(SO4)3和MgSO4 | D. | Na2SO4和MgSO4 |
| 钠的重要化合物. | |
| 专题: | 几种重要的金属及其化合物. |
| 分析: | 向无色溶液中加入过氧化钠,过氧化钠和水反应生成氢氧化钠和氧气,所以有无色无味的气体放出,并有白色沉淀 |
| 解答: | 解:A、向氯化钙和氯化镁溶液中加入过氧化钠,过氧化钠和水反应生成氢氧化钠和氧气,氢氧化钠和氯化镁反应生成氢氧化镁沉淀,当氢氧化钠过量时,氢氧化镁也不溶解,所以和图片不符,故A错误. B、向硫酸铝溶液中加入过氧化钠,过氧化钠和水反应生成氢氧化钠和氧气,氢氧化钠和铝离子反应生成氢氧化铝沉淀,当氢氧化钠过量时,氢氧化铝和氢氧化钠反应生成可溶性的偏铝酸钠,所以最终没有沉淀生成,与图片不符,故B错误. C、向硫酸铝和硫酸镁溶液中加入过氧化钠,过氧化钠和水反应生成氢氧化钠和氧气,氢氧化钠和铝离子反应生成氢氧化铝沉淀,当氢氧化钠过量时,氢氧化铝和氢氧化钠反应生成可溶性的偏铝酸钠,氢氧化钠和氯化镁反应生成氢氧化镁沉淀,当氢氧化钠过量时,氢氧化镁也不溶解,所以与图片相符,故C正确. D、向硫酸钠和硫酸镁溶液中加入过氧化钠,过氧化钠和水反应生成氢氧化钠和氧气,氢氧化钠和氯化镁反应生成氢氧化镁沉淀,当氢氧化钠过量时,氢氧化镁也不溶解,硫酸钠和氢氧化钠不反应,所以和图片不符,故D错误. 故选C. |
| 点评: | 本题考查了钠的化合物、氢氧化铝的性质,明确氢氧化铝的两性是解本题的关键,难度不大. |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
(Ⅰ)某二元酸(H2A)在水中的电离方程式是:H2A===H++HA-,HA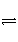
 -H++A2-。
-H++A2-。
(1)Na2A溶液显________(填“酸性”、“中性”或“碱性”)。理由是
________________________________________________________________________
(用离子方程式表示)。
(2)已知0.1 mol/L NaHA溶液的pH=2,则0.1 mol/L H2A溶液中氢离子的物质的量浓度应______0.11 mol/L(填“<”、“>”或“=”),理由是
________________________________________________________________________
________________________________________________________________________。
(Ⅱ)25℃时,A酸溶液的pH=a,B碱溶液的pH=b。
(1)若A为强酸,B为强碱,且a+b=14,若两者等体积混合后,溶液的pH=________,此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是
________________________________________________________________________。
(2)若A的化学式为HR,B的化学式为MOH,且a+b=14,两者等体积混合后溶液显酸性,则混合溶液中必定有一种离子能发生水解,该离子为__________(填离子符号);混合后的溶液中,下列微粒浓度大小关系一定正确的是____________(填序号)。
①c(MOH)>c(M+)>c(R-)>c(H+)>c(OH-)
②c(HR)>c(M+)>c(R-)>c(OH-)>c(H+)
③c(R-)>c(M+)>c(H+)>c(OH-)
④c(M+)>c(R-)>c(OH-)>c(H+)
⑤c(M+)+c(H+)=c(R-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
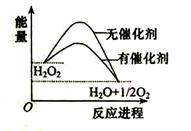 已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如下图所示。下列说法正确的是( )
已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如下图所示。下列说法正确的是( )
A.加入催化剂,减小了反应的热效应
B.加入催化剂,可提高H2O2的平衡转化率
C.H2O2分解的热化学方程式:H2O2 → H2O + O2 + Q
D.反应物的总能量高于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
已知水和苯互不相溶,苯不与钠反应,在烧杯中加水和苯(密度:0.88g/cm3)各50mL.将一小粒金属钠(密度:0.97g/cm3)投入烧杯中,观察到的现象可能是()
| A. | 钠在水层中反应并四处游动 | |
| B. | 钠停留在苯层中不发生反应 | |
| C. | 钠在苯的液面上反应并四处游动 | |
| D. | 钠在苯与水的界面处反应并可能做上、下跳动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定体积的CO2通入V L NaOH溶液中,已知NaOH完全反应,若在反应后的溶液中加入足量石灰水,得到a g沉淀;若在反应后的溶液中加入足量CaCl2溶液,得到b g沉淀,则下列说法正确的是()
| A. | 参加反应的CO2的体积为0.224a L | |
| B. | 用上述数据不能确定NaOH溶液的物质的量浓度 | |
| C. | 若a=b,则CO2与NaOH溶液反应的产物盐只有Na2CO3 | |
| D. | b可能等于a、小于a或大于a |
查看答案和解析>>
科目:高中化学 来源: 题型:
热化学方程式C(s)+H2O(g)===CO(g)+H2(g) ΔH=+131.3 kJ·mol-1表示( )
A.碳和水反应吸收131.3 kJ能量
B.1 mol碳和1 mol水反应生成1 mol一氧化碳和1 mol氢气并吸收131.3 kJ热量
C.1 mol固态碳和1 mol水蒸气反应生成1 mol一氧化碳气体和1 mol氢气并吸收131.3 kJ热量
D.1个固态碳原子和1分子水蒸气反应吸热131.3 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
已知强酸与强碱在稀溶液里反应的中和热可表示为
H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1
对下列反应:
CH3COOH(aq)+NaOH(aq)===CH3COONa(aq)+H2O(l) ΔH=-Q1 kJ·mol-1
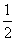 H2SO4(浓)+NaOH(aq)===
H2SO4(浓)+NaOH(aq)===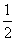 Na2SO4(aq)+H2O(l) ΔH=-Q2 kJ·mol-1
Na2SO4(aq)+H2O(l) ΔH=-Q2 kJ·mol-1
HNO3(aq)+NaOH(aq)===NaNO3(aq)+H2O(l)
ΔH=-Q3 kJ·mol-1
上述反应均在溶液中进行,则下列Q1、Q2、Q3的关系正确的是( )
A.Q2>Q3>Q1 B.Q2>Q1>Q3 C.Q1=Q2=Q3 D.Q2=Q3>Q1
查看答案和解析>>
科目:高中化学 来源: 题型:
煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式为:
a.C(s)+O2(g)===CO2(g) ΔH=E1①
b.C(s)+H2O(g)===CO(g)+H2(g) ΔH=E2②
H2(g)+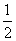 O2(g)===H2O(g) ΔH=E3③
O2(g)===H2O(g) ΔH=E3③
CO(g)+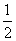 O2(g)===CO2(g) ΔH=E4④
O2(g)===CO2(g) ΔH=E4④
回答:
(1)上述四个热化学方程式中的哪些反应ΔH<0?
________________________________________________________________________。
(2)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是( )
A.a比b多 B.a比b少 C.a与b在理论上相同
(3)根据能量守恒定律,E1、E2、E3、E4之间的关系为
________________________________________________________________________
________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
两种烃A、B取等质量完全燃烧,生成CO2与消耗O2的量相同,这两种烃之间的关系正确的是( )
A.一定互为同分异构体
B.一定是同系物,有相同的通式
C.实验式相同
D.只能是同种物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com