
【题目】某化学兴趣小组想从FeI2溶液中获得碘单质,其设计流程如图。
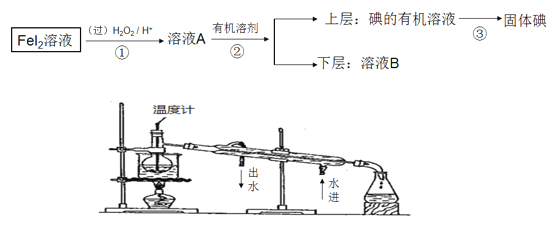
请回答:
(1)操作②中除烧杯外,还要用到的玻璃仪器的名称是________________
(2)有同学试图利用蒸馏方法来实现第③步操作,该同学设计了如图的实验装置,此装置中的明显错误是___________________________________
(3)溶液B呈黄色,除了含Fe3+,可能还含有I2,请你设计一个实验方案加以证明,你的实验操作方案是__________________________________________
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3 , 还含有Fe2O3、SiO2)提取氧化铝,冶炼铝的原料,提取的操作过程如图:
请回答下列问题:
(1)写出步骤①中发生反应的离子方程式;滤渣①的成分为 .
(2)写出步骤②中生成含铝化合物的化学方程式;能否将此步骤中的NaOH 溶液更换为氨水?(填“能”或“不能”).若不能,请说明理由:(若能,则此空不答).
(3)步骤③中的X 为(填化学式),发生反应的离子方程式为 .
(4)若铝土矿的质量为mkg,最后得到A12O3的质量为nkg(忽略提取过程中铝元素的损失),则铝土矿中铝元素的质量分数为(用含m、n 的代数式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X,Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( ) 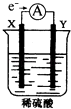
A.X极上发生的是还原反应
B.若两电极分别为Fe和碳棒,则Y为Fe
C.若反应进行一段时间后,产生2克H2时转移了1mol电子
D.溶液中的SO42﹣向X极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3COOOH(过氧乙酸)广泛应用于环境和医院手术室的消毒,某校化学兴趣小组想利用CH3COOH+H2O2=CH3COOOH+H2O来制取过氧乙酸,查得相关数据如下:
物质 | 沸点 ℃ | 熔点 ℃ | 溶解性 |
CH3COOH | 117.9 | 16.6 | 能溶于水及酒精等有机溶剂 |
H2O2 | 150.2 | -0.43 | 溶于水及酒精 |
CH3COOOH | 105 | 0.1 | 溶于水及酒精等有机溶剂 |
同时查得过氧乙酸具有:刺激性气味,易燃;加热至100℃即猛烈分解;遇火或受热、受震都可引起爆炸;对金属具有较强的腐蚀性。回答以下问题:
(1)利用如图装置进行制取,实验中水浴温度应控制在________100℃(填“>”或“<”或“=”),原因是:____________________________________________________________
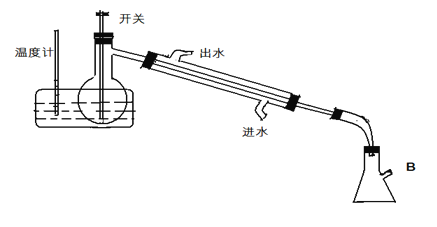
(2)为了使实验顺利进行,B处应接一个_________(填一种装置),然后缓慢打开图中开关通入空气,从而得到过氧乙酸溶液。
(3)实验结束后得到一定量的过氧乙酸,利用如下反应测定该产物的纯度:
2KMnO4+5H2O2 +3H2SO4=K2SO4+2MnSO4+8H2O+5O2↑
2KI+ CH3COOOH+2 H2SO4=2KHSO4+I2+ CH3COOH+H2O
I2+2Na2S2O3=2NaI+Na2S4O6
①取10.00mL制得的过氧乙酸溶液,加水稀释到1000mL,用移液管取20.00mL至锥形瓶中,加入足量稀硫酸酸化后,再用____________(填“酸式滴定管”或“碱式滴定管”)装0.100mol/L的KMnO4溶液进行滴定至_______________________________________现象时恰好完全反应,从而将混在过氧乙酸中的H2O2除去。然后再加入过量KI溶液,加入几滴淀粉,再用0.100mol/L的Na2S2O3滴定消耗了12.00mL。一般工业制得的过氧乙酸质量分数为18% ~ 23%。如果测得实验室制得的过氧乙酸溶液密度为1.15gcm-3。试通过计算判断该溶液是否合格_____________。
②滴定过程中,下列操作会使结果偏大的是_________。
A.滴加Na2S2O3时开始平视滴定管,结束时俯视滴定管。
B.装标准Na2S2O3溶液的滴定管未用标准Na2S2O3溶液润洗。
C.移液管在使用之前未用烘干,里面附着水珠就用来量取待测液
D. .滴加Na2S2O3时开始仰视滴定管,结束时平视滴定管。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡及其化合物在生产、生活中有着重要的用途。已知: Sn的熔点为231℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33℃、沸点为114℃。请回答下列问题:
(1)元素锡比同主族碳的周期数大3,锡的原子序数为_________。
(2)用于微电子器件生产的锡粉纯度测定(已知锡的相对原子质量为119): ①取1.19g试样溶于稀硫酸中(杂质不参与反应),使Sn 完全转化为Sn2+;②加入过量的Fe2(SO4)3;③用0.1000mol/LK2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00mL。步骤②中加入Fe2(SO4)3的作用是________;此锡粉样品中锡的质量分数为_________。若在滴定终点时俯视读数,则会导致测得的样品中锡的质量分数________(填“偏高“偏低”或“无影响”)。
(2)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:

①步骤I加入Sn粉的作用:____________及调节溶液pH。
②步骤II用到的玻璃仪器有烧杯、____________。
③步骤III生成SnO的离子方程式: ____________。
④步骤IV中检验SnO是否洗涤干净的操作是____________,证明已洗净。
⑤步骤V操作依次为____________ 、____________过滤、洗涤、低温干燥。
(4)实验室欲用下图装置制备少量SnCl4(夹持装置略),该装置存在明显缺陷,改进方法是____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要配制2.0mol/L的NaOH溶液950ml,配制时应选用的容量瓶的规格和称取NaOH的质量分别是
A. 950ml,76.0g B. 500ml,,80g
C. 1000ml,76.0g D. 1000ml,80.0g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
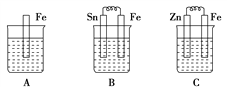
①B中Sn极的电极反应式为_______;Sn极附近溶液的pH(填“增大”、“减小”或“不变”)______。
②C中总反应离子方程式为_______________。
③比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是________________。
(2)如图是甲烷燃料电池原理示意图,回答下列问题:
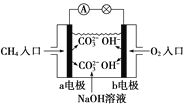
①电池的负极是________(填“a”或“b”)电极,该极的电极反应是:_______________________。
②常温下,如果该原电池电解质溶液为pH=13的氢氧化钠500mL,构成原电池一段时间后pH变为12,则构成原电池消耗了标准状况下__________ mL甲烷,(假设化学能全部转化为电能,忽略氢氧化钠溶液的体积变化)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com