
| A. | SO2在葡萄糖中作抗氧化剂 | B. | Fe3O4常用作红色油漆和涂料 | ||
| C. | SiO2可制成太阳能电池 | D. | 漂粉精可用于游泳池的消毒 |
分析 A.二氧化硫有毒;
B.四氧化三铁为黑色固体;
C.二氧化硅传导光信号;
D.漂粉精是次氯酸盐,具有强氧化性,能消毒杀菌.
解答 解:A.二氧化硫有还原作用,可消耗果蔬组织中的氧,破坏其氧化酶系统,故有抗氧化作用,但二氧化硫有毒,一般不用于直接食用的葡萄糖中,故A错误;
B.四氧化三铁为黑色固体,不能用作红色油漆和涂料,应该是Fe2O3,故B错误;
C.二氧化硅可传导光信号,可用作光纤,不能用作太阳能电池,硅是良好的半导体材料,硅才是制造太阳能电池的重要原料,故C错误;
D.漂粉精是次氯酸盐,在水溶液中水解生成次氯酸,具有强氧化性,能消毒杀菌,故D正确;
故选D.
点评 本题综合考查物质的性质以及应用,为高频考点,侧重于化学与生活、生产的考查,有利于培养学生良好的科学素养,注意把握常见物质的性质与用途的关系,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 髙炉炼铁 | B. | 硅胶作袋装食品的干燥剂 | ||
| C. | 天然气作燃料 | D. | 肥皂水作蚊虫叮咬处的淸洗剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9.3 | B. | 9.7 | C. | 10 | D. | 10.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
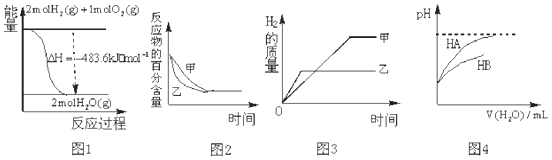
| A. | 图 1 表示 H2与O2发生反应过程中的能量变化,则H2的燃烧热为 241.8kJ•mol-1 | |
| B. | 图 2 表示压强对可逆反应 2A(g)+2B (g)?3C(g)+D(s)的影响,乙的压强比甲的压强大 | |
| C. | 图 3 表示等质量的钾、钠分别与足量水反应,则甲为钠 | |
| D. | 图 4 表示常温下,稀释 HA、HB 两种酸的稀溶液时,溶液 pH 随加水量的变化,则相同条件下 NaA溶液的 pH 大于同浓度的 NaB 溶液的 pH. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 原因 | 结论 |
| A | 乙烯和苯都能使溴水褪色 | 苯分子和乙烯分子含有相同的碳碳双键 |
| B | 乙酸分子中含有羧基 | 可与NaHCO3溶液反应生成CO2 |
| C | 乙醇是电解质 | 乙醇可与钠反应放出氢气 |
| D | 乙酸乙酯和乙烯在一定条件下都能与水反应 | 二者属于同一反应类型 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 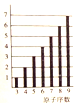 图纵坐标为元素的最高正价 | |
| B. |  图可说明反应2NO+2CO=N2+2CO2为吸热反应 | |
| C. | 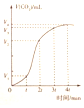 若图表示的是一定量的CaCO3与盐酸反应生成CO2的体积随时间的变化,则t~2tmin反应速率最快 | |
| D. | 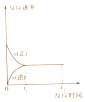 若图表示的是反应N2(g)+3H2(g)?2NH3(g)的.v(正)、v(逆)随时间的变化,则0~t1时间段:v(正)=v(逆) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
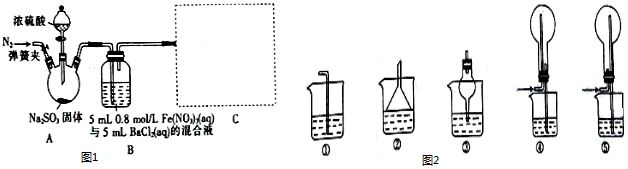
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
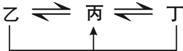 已知A、B、C、D、E、F是原子序数依次增大的前四周期元素,A与C同主族,A与B、A与E形成共价化合物,A与B形成的最简单化合物的水溶液呈碱性,E的最高正化合价与最低负化合价的代数和为4,D是同周期中简单离子半径最小的元素,F元素对应的单质为日常生活中常见金属.
已知A、B、C、D、E、F是原子序数依次增大的前四周期元素,A与C同主族,A与B、A与E形成共价化合物,A与B形成的最简单化合物的水溶液呈碱性,E的最高正化合价与最低负化合价的代数和为4,D是同周期中简单离子半径最小的元素,F元素对应的单质为日常生活中常见金属. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com